题目内容
【题目】分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中所有碳原子都在同一平面上
B. 可与乙醇、乙酸反应且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
【答案】B
【解析】A.与-OH、醚键相连的环状结构上C(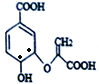 )为四面体结构,则所有原子不可能共面,故A错误;B.含-COOH与乙醇发生酯化反应,含-OH与乙酸发生酯化反应,故B正确;C.不含苯环,只有-COOH与NaOH反应,则1mol分枝酸最多可与2molNaOH发生中和反应,故C错误;D.碳碳双键与溴的四氯化碳溶液发生加成反应,双键与-OH均能被酸性高锰酸钾溶液氧化,原理不同,故D错误;故选B。
)为四面体结构,则所有原子不可能共面,故A错误;B.含-COOH与乙醇发生酯化反应,含-OH与乙酸发生酯化反应,故B正确;C.不含苯环,只有-COOH与NaOH反应,则1mol分枝酸最多可与2molNaOH发生中和反应,故C错误;D.碳碳双键与溴的四氯化碳溶液发生加成反应,双键与-OH均能被酸性高锰酸钾溶液氧化,原理不同,故D错误;故选B。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
【实验Ⅰ】试剂:酸化的0.5 mol·L-1FeSO4溶液(pH = 0.2),5% H2O2溶液(pH = 5)
操作 | 现象 |
取2mL上述FeSO4溶液于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液pH=0.9 |
向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(1)H2O2的电子式是_______,上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是________。
(2)产生气泡的原因是____________________。
【实验Ⅱ】 试剂:未酸化的0.5 mol·L-1FeSO4溶液(pH = 3),5% H2O2溶液(pH = 5)
操作 | 现象 |
取2 mL5% H2O2溶液于试管中,加入5滴上述FeSO4溶液 | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液pH=1.4 |
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加4mol·L-1盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有Fe2O3,经检验还含有SO42-。检验棕黄色沉淀中SO42-的方法是________。
(4)对于生成红褐色胶体的原因,提出两种假设:
i.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+ 氧化的产物发生了水解
① 根据实验II记录否定假设i,理由是________。
② 实验验证假设ii:取Fe2(SO4)3溶液加热,溶液变为红褐色,pH下降,证明假设ii成立。
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是________。
【实验Ⅲ】
若用FeCl2溶液替代FeSO4溶液,其余操作与实验II相同,除了产生与II相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是________。
(7)由实验Ⅰ、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与________(至少写两点)有关。
【题目】某同学用某种粗盐进行提纯实验,步骤见下图。请回答:
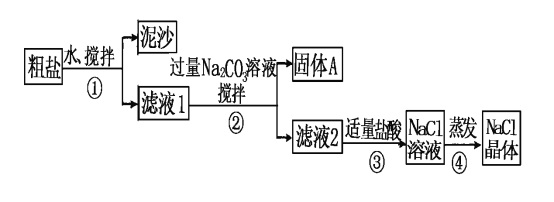
(1)步骤①和②的操作名称是________________。
(2)步骤②中判断加入碳酸钠是否过量的方法是_____________________
步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止__________________,当蒸发皿中有较多量固体出现时,应___________________________________。
(3)猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | ___________ | 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入________,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想Ⅱ不成立 |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,__________ | __________________ | 猜想Ⅲ成立 |
(4)写出“猜想Ⅲ”中对应的化学反应方程式:______________________________