题目内容
下列实验操作方法及结论都正确的是( )
| A、向某溶液中加AgNO3溶液产生白色沉淀,证明有Cl- |
| B、把H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,证明H2O2有还原性 |
| C、向某溶液中加入稀 HCl,放出能使澄清的石灰水变浑浊的气体,证明有CO32- |
| D、向某溶液中加稀盐酸,无现象,再加入BaCl2溶液产生白色沉淀,证明有SO42- |
考点:化学实验方案的评价
专题:实验评价题
分析:A.和硝酸银溶液反应生成白色沉淀的离子不一定是氯离子;
B.H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,则亚铁离子生成铁离子,双氧水生成水,据此判断双氧水的性质;
C.能使澄清石灰水变浑浊的气体不一定是二氧化碳,能和稀盐酸反应生成二氧化碳的离子不一定是碳酸根离子;
D.用盐酸酸化的氯化钡溶液具有硫酸根离子.
B.H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,则亚铁离子生成铁离子,双氧水生成水,据此判断双氧水的性质;
C.能使澄清石灰水变浑浊的气体不一定是二氧化碳,能和稀盐酸反应生成二氧化碳的离子不一定是碳酸根离子;
D.用盐酸酸化的氯化钡溶液具有硫酸根离子.
解答:
解:A.和硝酸银溶液反应生成白色沉淀的离子不一定是氯离子,可能是碳酸根离子,故A错误;
B.H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,则亚铁离子生成铁离子,双氧水生成水,双氧水中的O元素化合价由-1价变为-2价,所以双氧水作氧化剂,则双氧水体现氧化性,故B错误;
C.能使澄清石灰水变浑浊的气体有二氧化硫和二氧化硫,能和稀盐酸反应生成二氧化碳的离子有碳酸根离子和碳酸氢根离子,故C错误;
D.用盐酸酸化的氯化钡溶液具有硫酸根离子,稀盐酸除去碳酸根离子、亚硫酸根离子的干扰,硫酸根离子和钡离子反应生成不溶于稀盐酸的白色沉淀,故D正确;
故选D.
B.H2O2滴入FeCl2溶液中,溶液由浅绿色变为棕黄色,则亚铁离子生成铁离子,双氧水生成水,双氧水中的O元素化合价由-1价变为-2价,所以双氧水作氧化剂,则双氧水体现氧化性,故B错误;
C.能使澄清石灰水变浑浊的气体有二氧化硫和二氧化硫,能和稀盐酸反应生成二氧化碳的离子有碳酸根离子和碳酸氢根离子,故C错误;
D.用盐酸酸化的氯化钡溶液具有硫酸根离子,稀盐酸除去碳酸根离子、亚硫酸根离子的干扰,硫酸根离子和钡离子反应生成不溶于稀盐酸的白色沉淀,故D正确;
故选D.
点评:本题考查了化学实验方案评价,涉及物质或离子的检验,明确物质的性质是解本题关键,知道氯离子、硫酸根离子的检验方法、试剂及现象,要排除其它离子的干扰,题目难度不大.

练习册系列答案
相关题目
下列关于卤代烃的说法正确的是( )
| A、在溴乙烷(CH3CH2Br)分子中,溴元素的存在形式为溴离子 |
| B、在卤代烃中,卤素原子与碳原子形成共价键 |
| C、聚四氟乙烯(塑料王)为高分子化合物,不属于卤代烃 |
| D、卤代烃比相应的烷烃的沸点低 |
下列反应属于加成反应的是( )
A、C3H8+Cl2
| |||
| B、2FeCl2+Cl2═2FeCl3 | |||
C、CH2═CH2+H2O
| |||
D、CH3CH2OH
|
下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A、相同物质的量浓度的下列溶液:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3?H2O,c(NH4+)由大到小的顺序是:①>④>②>③ |
| B、常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
| C、常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7mol?L-1 |
| D、物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:C(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-) |
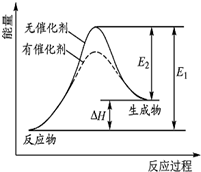 某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、该反应焓变可表示为△H=-(E1-E2)kJ?mol-1 |
| C、催化剂能降低反应的活化能 |
| D、催化剂能改变反应的焓变 |
在CH3COCH3中,中间的碳原子与两边的碳原子成键所用的轨道是( )
| A、SP2-SP2 |
| B、SP3-SP3 |
| C、SP2-SP3 |
| D、SP-SP3 |
下列说法中正确的是( )
| A、乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能为同分异构体 |
| B、二氧化碳和干冰互为同素异形体 |
| C、C2H5OH和CH3OCH3互为同分异构体 |
| D、金刚石和石墨互为同位素 |