题目内容
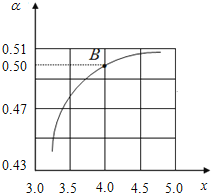
【题目】已知:还原性HSO3->I-,氧化性IO3->I2。在含3mol NaHSO3的溶液中逐滴加人KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是

A. 0-a段发生反应:3HSO3-+IO3-=3SO42-+I-+3H+
B. a~b段共消耗NaHSO3的物质的量为1.8mol
C. b~c段反应:氧化产物为I2
D. 当溶液中I-与I2的物质的量之比为5 : 1时,加入的KIO3为1.lmol
【答案】D
【解析】还原性HSO-3>I-,所以首先发生:IO3-+3HSO3-=I-+3SO42-+3H+,继续加入NaIO3,由于氧化性IO-3>I2,所以IO3-可以结合H+氧化I-生成I2,离子方程式是IO3-+6H++5I-=3H2O+3I2。A、根据以上分析可知0~a段发生反应:3HSO3-+ IO3-=3SO42-+I-+3H+,A正确;B、a点碘酸钠的物质的量是0.4mol,根据碘酸钠和亚硫酸氢钠的关系式知,消耗NaHSO3的物质的量=![]() ×3=1.2mol,则a点时剩余NaHSO3的物质的量为1.8 mol,因此a~b段共消耗NaHSO3的物质的量为1.8mol,B正确;C、根据以上分析可知b~c段反应:IO3-+6H++5I-=3H2O+3I2,氧化产物为I2,C正确;D、根据反应IO3-+3HSO3-=I-+3SO42-+3H+,3mol NaHSO3的溶液消耗NaIO3溶液的物质的量为1mol,生成碘离子的量为1mol,设生成的碘单质的物质的量为n,则根据反应IO3-+6H++5I-=3H2O+3I2,消耗的NaIO3的物质的量为
×3=1.2mol,则a点时剩余NaHSO3的物质的量为1.8 mol,因此a~b段共消耗NaHSO3的物质的量为1.8mol,B正确;C、根据以上分析可知b~c段反应:IO3-+6H++5I-=3H2O+3I2,氧化产物为I2,C正确;D、根据反应IO3-+3HSO3-=I-+3SO42-+3H+,3mol NaHSO3的溶液消耗NaIO3溶液的物质的量为1mol,生成碘离子的量为1mol,设生成的碘单质的物质的量为n,则根据反应IO3-+6H++5I-=3H2O+3I2,消耗的NaIO3的物质的量为![]() mol,消耗碘离子的量为
mol,消耗碘离子的量为![]() mol,剩余的碘离子为(1-
mol,剩余的碘离子为(1-![]() )mol,当溶液中n(I-):n(I2)=5:1时,即(1-
)mol,当溶液中n(I-):n(I2)=5:1时,即(1-![]() )mol:nmol=5:1,故n=0.15mol,故加入的n(NaIO3)=1mol+
)mol:nmol=5:1,故n=0.15mol,故加入的n(NaIO3)=1mol+![]() mol=1mol+0.05mol=1.05mol,D错误,答案选D。
mol=1mol+0.05mol=1.05mol,D错误,答案选D。

【题目】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO2(g)![]() 2NO(g)+O2 (g) (正反应吸热)。实验测得: v正= v(NO2)消耗=k正c2(NO2 ),v逆= v(NO)消耗=2v(O2)消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。下列说法正确的是
2NO(g)+O2 (g) (正反应吸热)。实验测得: v正= v(NO2)消耗=k正c2(NO2 ),v逆= v(NO)消耗=2v(O2)消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。下列说法正确的是
容器编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
I | 0.6 | 0 | 0 | 0.2 |
II | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 达平衡时,容器I与容器Ⅱ中的总压强之比为 4∶5
B. 达平衡时,容器中Ⅱ中 c(O2)/ c(NO2) 比容器I中的大
C. 达平衡时,容器Ⅲ中NO的体积分数小于50%
D. 当温度改变为 T2时,若 k正=k逆,则 T2<T1
【题目】一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生如下反应:PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
编号 | 温度(℃) | 起始物质的量 | 平衡物质的量 | 达到平衡所需时间 | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ<容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)=![]() mol·L-1·s-1
mol·L-1·s-1
D.起始时向容器Ⅲ中充入PCl50.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行