题目内容
将0.4mol丁烷完全燃烧后生成的气体全部缓慢通人1L 2mol/LNaOH溶液中,生Na2CO3和NaHCO3的物质的量之比为
| A.3:2 | B.2:3 | C.2:1 | D.1:3 |
D
解析试题分析:据碳原子个数守恒可知,0.4摩尔丁烷可以生成1.6摩尔的二氧化碳。1L 2mol/LnaOH的物质的量为2摩尔。而二氧化碳与氢氧化钠反应生成碳酸钠,二氧化碳过量,因此应以氢氧化钠的量为基准进行计算。列出反应方程式可知,消耗的氢氧化钠与二氧化碳的量之比为2;1,因此会生成1摩尔的碳酸钠,同时还剩下0.6摩尔的二氧化碳。而剩余的0.6摩尔二氧化碳可以与0.6摩尔的碳酸钠继续反应生成1.2摩尔的碳酸氢钠,因此还剩余的碳酸钠就为1减去0.6等于0.4摩尔。所以碳酸钠与碳酸氢钠的物质的量之比就为1;3的关系,所以答案选D
考点:考查有机物的相关计算

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则氢元素的质量分数为
| A.11% | B.28% | C.54% | D.9% |
目前,世界上已合成了几百万种的有机超导体,TCNQ是其中之一。TCNQ的分子结构如图,下列关于TCNQ的说法错误的是( )
| A.TCNQ分子中所有原子可能都在同一平面上 |
| B.TCNQ属于苯的同系物 |
| C.TCNQ分子中既存在极性键又存在非极性键 |
| D.1mol TCNQ在一定条件下最多能和12molH2反应 |
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可转化成以下多种化合物(如下图)。下列说法正确的是
| A.正四面体烷的分子式为C4H4,其二氯代物有二种 |
| B.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 |
| C.苯为平面六边形结构,分子中存在C—C和C=C,能使KMnO4溶液褪色 |
| D.环辛四烯不能使溴水褪色 |
下列与有机物结构、性质相关的叙述错误的是 ( )
A.乙醛和丙烯醛( )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B.一分子β-月桂烯( )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C.用甘氨酸( )和丙氨酸( )和丙氨酸( )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D. 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示: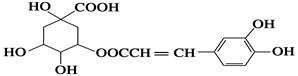
关于咖啡鞣酸的下列叙述正确的是 ( )
| A.分子式为C16H13O9 |
| B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应 |
| C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键 |
| D.与浓溴水能发生两种类型的反应 |
三氯生是一种抗菌剂,其结构如图所示,它遇含氯自来水能生成有毒的三氯甲烷。下列说法不正确的是
| A.三氯生的分子式是C12H6Cl3O2 |
| B.三氯甲烷与甲烷均无同分异构体 |
| C.1 摩三氯生最多能与6 mol H2反应 |
| D.1摩三氯生最多能与7 mol NaOH反应 |
为提纯下列物质(括号内为杂质).所选试剂及方法均正确的是
| 选项 | 物质(括号内为杂质) | 除杂试剂 | 方法 |
| A | 溴苯(溴) | CCl4 | 分液 |
| B | 硝基苯(NO2) | NaOH溶液 | 分液 |
| C | 乙烷(乙烯) | 氢气 | 洗气 |
| D | 乙醇(乙酸) | NaOH溶液 | 分液 |
