题目内容
【题目】向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。有关说法不正确的是
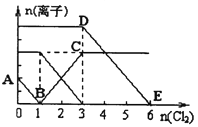
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中n(FeBr2)=6mol
C.当通入Cl22mol时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2C12=2Fe3++I2+4Cl-
D.原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3
【答案】B
【解析】
试题分析:还原性为I->Fe2+>Br-,则先发生2 I-+Cl2═I2+2Cl-,I-反应完毕再发生2Fe2++C12=2Fe3++2Cl-,最后发生反应2Br-+Cl2=Br2+2Cl-。A.B点时溶液中I-完全反应,溶液中存在Fe2+和Br-,BC段发生2 Fe2++Cl2=2Fe3++2Cl-,代表Fe3+的物质的量的变化情况,正确;B.由图可知,BC段发生2Fe2++C12= 2Fe3++2Cl-,Fe2+反应完毕消耗氯气2mol,由方程式可知n(Fe2+)=2×2mol=4mol,则n(FeBr2)==4mol,错误;C.AB段发生2 I-+Cl2═I2+2Cl-,2mol的I-消耗1mol氯气,BC段发生2Fe2++C12=2Fe3++2Cl-,余下的1mol氯气再与2mol Fe2+反应,故参加反应的n(Fe2+):n(I-)=1:1,故通入2molCl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2C12=2Fe3++I2+4Cl-,正确;D.由图可知AB段消耗氯气1mol,发生2 I-+Cl2═I2+2Cl-,,故n(I-)=2n(Cl2)=2mol,BC段发生2Fe2++C12=2Fe3++2Cl-,消耗氯气2mol,故n(Fe2+)= 2n(Cl2)==2×2mol=4mol,DE段发生2Br-+Cl2=Br2+2Cl-,消耗氯气3mol,故n(Br-)=2n(Cl2)=6mol,故原溶液中n(Fe2+):n(I-):n(Br-)=4mol:2mol:6mol=2:1:3,正确。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】一定温度下,2L密闭容器中充入0.40 mol N2O4,发生反应:N2O4(g)![]() 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
请回答:
(1)20 s内,v(NO2)=____________mol·L-1·s-1。
(2)升高温度时,气体颜色加深,则正反应是____________(填“放热”或“吸热”)反应。
(3)该温度下反应的化学平衡常数数值为_____________。
(4)相同温度下,若开始时向该容器中充入的是0.20 molN2O4和0.40molNO2,则达到平衡后,c(NO2)=_____________。