题目内容
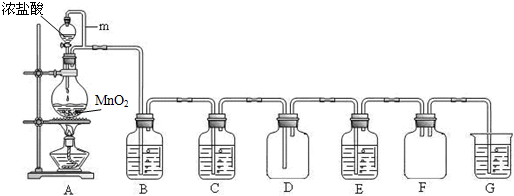
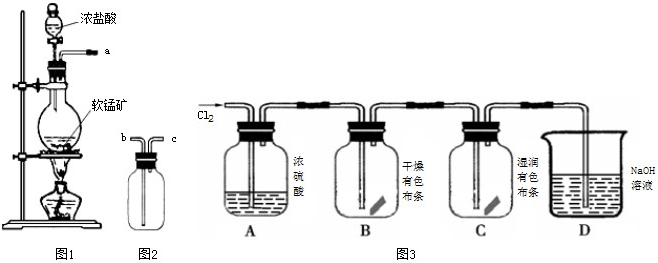
(10分)二氧化锰(MnO2)与浓盐酸混合加热可得到氯气,下图是制取并探究Cl2化学性质的装置图。

(1)圆底烧瓶中发生反应的化学方程式为 。
(2)A 中m 管的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是 。
(4)E中若装有FeCl2 溶液,反应的离子方程式为 ;E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,长郡中学高二化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体,加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2 中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ;
实验c的目的是 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。
(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O(2分)
MnCl2+Cl2↑+2H2O(2分)
(2)连通圆底烧瓶和分液漏斗,平衡压强,使分液漏斗中的液体顺利流下(2分)
(3)饱和食盐水(1分)、
(4)2Fe2++Cl2===2Fe3++2Cl-(1分) 溶液变蓝(1分)
(5)①探究c(Cl-)对反应的影响(1分)
探究c(H+)对反应的影响(1分)
②c(H+)的大小(1分)
【解析】

 阅读快车系列答案
阅读快车系列答案