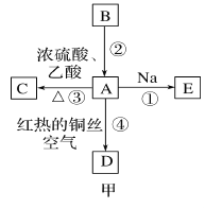
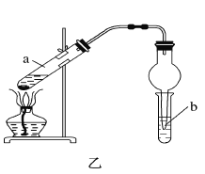
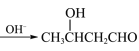题目内容
【题目】SiHCl3在催化剂作用下主要发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g) ΔH=+48kJ·mol-1。已知:反应速率
SiH2Cl2(g)+SiCl4(g) ΔH=+48kJ·mol-1。已知:反应速率![]() ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。

下列说法正确的是( )
A.343K时反应物的平衡转化率为21%
B.a点的反应速率小于b点的反应速率
C.343K时![]() =
=![]()
D.由323K的平衡转化率数据,不能计算323K的平衡常数K
【答案】C
【解析】
分析题给信息,该可逆反应为气体分子数不变且吸热的反应。则对于该可逆反应来说,温度升高,反应向正反应方向进行。根据题中t-SiHCl3%图,可知曲线a为343K时SiHCl3的转化率-时间曲线,曲线b为323K时SiHCl3的转化率-时间曲线。据此进行分析。
A.由分析可知,曲线a为343K时的变化曲线,由图可知,343K时反应物的平衡转化率为22%,A项错误;
B.由图可知,a、b两点的转化率相等,可认为各物质的浓度对应相等,而a点的温度更高,所以速率更快,即a点的反应速率大于b点的反应速率,B项错误;
C.由图可知,343K时SiHCl3的转化率为22%,设起始时SiHCl3的浓度为1mol/L,则根据反应方程式有:

平衡时v正=v逆,则![]() ,则
,则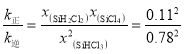 ,C项正确;
,C项正确;
D.由图可知,323K时SiHCl3的转化率为21%,设起始时SiHCl3的浓度为1mol/L,由反应方程式可知:

该可逆反应的平衡常数K=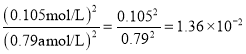 ,故由323K的平衡转化率数据,可以计算323K的平衡常数K,D项错误;
,故由323K的平衡转化率数据,可以计算323K的平衡常数K,D项错误;
答案选C。

【题目】下图是元素周期表的一部分,根据① ~ ⑨在周期表中的位置按题目要求回答:
族 周期 | IA | 0 | ||||||||
1 | ⅡA | …… …… …… | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
2 | ① | ② | ||||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||||
4 | ⑧ | ⑨ | ⑩ | |||||||
(1)画出⑩的原子结构示意图_________________________
(2)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的结构式 __________________________________。
(3)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式__________________。
(4)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程__________________。
(5)②、⑥分别形成的两种氢化物中,沸点较高的是______(填化学式),原因是:___________________________________________________ 。