题目内容
在一定温度下将1mol CO(g)和1mol H2O(g)通入一个容积固定的密闭容器中反应:CO(g)+H2O(g)?CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是( )
分析:CO(g)+H2O(g)?CO2(g)+H2(g),
开始 1 1 0 0
转化0.6 0.6 0.6 0.6
平衡 0.4 0.4 0.6 0.6
再通入4molH2O(g),平衡正向移动,但CO不能完全转化,以此来解答.
开始 1 1 0 0
转化0.6 0.6 0.6 0.6
平衡 0.4 0.4 0.6 0.6
再通入4molH2O(g),平衡正向移动,但CO不能完全转化,以此来解答.
解答:解:CO(g)+H2O(g)?CO2(g)+H2(g),
开始 1 1 0 0
转化0.6 0.6 0.6 0.6
平衡 0.4 0.4 0.6 0.6
再通入4molH2O(g),平衡正向移动,但CO不能完全转化,
则再次达到平衡后,CO2的物质的量大于0.6mol,小于1mol,
故选D.
开始 1 1 0 0
转化0.6 0.6 0.6 0.6
平衡 0.4 0.4 0.6 0.6
再通入4molH2O(g),平衡正向移动,但CO不能完全转化,
则再次达到平衡后,CO2的物质的量大于0.6mol,小于1mol,
故选D.
点评:本题考查化学平衡的计算,注意平衡时CO的物质的量及加4molH2O(g)平衡正向移动,但CO不能完全转化为解答的关键,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
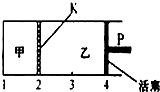 已知可逆反应:A(s)+2B(g)═C(g)+D(g)△H<0.在一定温度下将1mol A和2molB加入如图所示甲容器中,将2molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( )
已知可逆反应:A(s)+2B(g)═C(g)+D(g)△H<0.在一定温度下将1mol A和2molB加入如图所示甲容器中,将2molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( )| A、保持乙中压强不变,升高温度,达到新的平衡后,乙中平均相对分子质量增大 | B、保持温度和乙中压强不变,向乙中再加入2 mol D,达到新平衡后,一定有c(B)乙>c(B)甲 | C、若该温度下反应的K=1,则甲中B和乙中C的转化率均为66.7% | D、保持温度和活塞位置不变,甲中再加入1 mol A和2mol B,达到新的平衡后,c(B)甲=2c(B)乙 |
 (2011?常州三模)已知可逆反应:A(s)+2B(g)?C(g)+D(g)△H<0.在一定温度下将1mol A和2molB加入如图所示甲容器中,将2molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( )
(2011?常州三模)已知可逆反应:A(s)+2B(g)?C(g)+D(g)△H<0.在一定温度下将1mol A和2molB加入如图所示甲容器中,将2molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,在恒温下使两容器内反应均达到平衡状态(如图所示,隔板K不能移动).下列说法正确的是( ) CO2(g)+H2(g)达到平衡后,测得CO2为0.75mol,再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和为( )
CO2(g)+H2(g)达到平衡后,测得CO2为0.75mol,再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和为( )