题目内容
【题目】下列离子方程式中,属于盐类水解反应的是
A. Na2CO3溶液:CO32- + 2H2O ![]() H2CO3 + 2OH-
H2CO3 + 2OH-
B. NaHCO3溶液:HCO3- + H2O ![]() CO32- + H3O+
CO32- + H3O+
C. NaHS溶液:HS- + H2O ![]() H2S + OH-
H2S + OH-
D. KF溶液:F- + H2O = HF + OH-
【答案】C
【解析】
A. 碳酸是二元弱酸,多元弱酸的强碱盐的水解是分步进行的,不能合并,以第一步为主,故A错误;
B. HCO3-水解的离子方程式:HCO3-+H2OH2CO3+OH-,故B错误;
C. NaHS溶液,HS-水解的离子方程式:HS-+H2OH2S+OH-,故C正确;
D. KF溶液,F-水解的离子方程式:F-+H2O![]() HF+OH-,应使用可逆符号,故D错误,
HF+OH-,应使用可逆符号,故D错误,
故选C。

练习册系列答案
相关题目
【题目】下列实验操作对应的现象符合事实的是( )
|
|
|
|
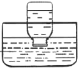
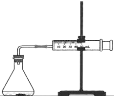
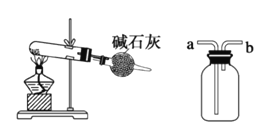
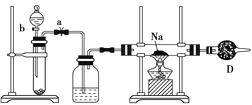
A.将绿豆大小的金属钠投入蒸馏水中,钠块熔成小球,浮于水面,迅速游 动,溶液变红 | B.将甲烷与氯气1∶1混合,在光照条件下反应,黄绿色褪去,水面上升,充满集气瓶 | C.将5g碳酸钙投入20mL1mol·L-1盐酸,针筒活塞向右移动的速率先逐渐增大,然后减小 | D.将铜片与浓硫酸混合加热,品红溶液变红,试管内出现蓝色固体和 少量黑色物质 |
A.AB.BC.CD.D