题目内容
下列有关物质的熔点的比较中,不正确的是

| A.晶体Si < 金刚石 | B.CO2 < SiO2 | C. NaCl < NaBr | D. PH3 < NH3 |
C
A 正确,原子晶体中,半径越小,熔点越高,碳原子的半径比硅原子的半径小,金刚石的熔点就高。
B 正确,原子晶体的熔点大于分子晶体的熔点。
C 错误,离子晶体中,半径越小,熔点越高,氯原子的半径小于溴原子的半径,故NaCl >NaBr
D 正确,氨气中存在氢键,所以,PH3 < NH3
B 正确,原子晶体的熔点大于分子晶体的熔点。
C 错误,离子晶体中,半径越小,熔点越高,氯原子的半径小于溴原子的半径,故NaCl >NaBr
D 正确,氨气中存在氢键,所以,PH3 < NH3

练习册系列答案
相关题目
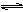 CH3CH2OH(g)+3H2O(g) △H=a kJ·mol-1
CH3CH2OH(g)+3H2O(g) △H=a kJ·mol-1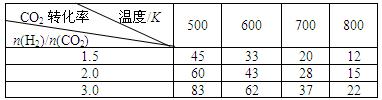
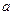 0(填“大于”或“小于”)。
0(填“大于”或“小于”)。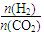 )比,平衡常数K值 (填“增大”、“减小”、或“不变”),对生成乙醇 (填“有利”或“不利”)。
)比,平衡常数K值 (填“增大”、“减小”、或“不变”),对生成乙醇 (填“有利”或“不利”)。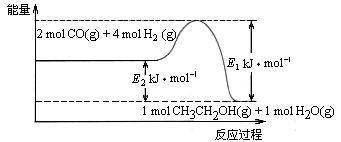


 表示,阴离子B以
表示,阴离子B以 表示。则每个晶胞中含A离子的数目为________,含B离子数目为________。若A的核外电子排布与Ar相同,B的核外电子排布与Ne相同,则该离子化合物的化学式是___________________;
表示。则每个晶胞中含A离子的数目为________,含B离子数目为________。若A的核外电子排布与Ar相同,B的核外电子排布与Ne相同,则该离子化合物的化学式是___________________;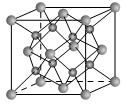
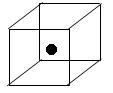

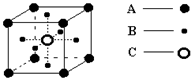

 为5. 71g·cm-3,晶胞边长为4.28×10-10m(Ni的相对原子质量为58.7,O的相对原子质量为16)。求:(已知:4.283="78.4 "
为5. 71g·cm-3,晶胞边长为4.28×10-10m(Ni的相对原子质量为58.7,O的相对原子质量为16)。求:(已知:4.283="78.4 " 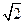 =1.4)
=1.4)