题目内容
【题目】减排是各个国家都在努力为之的事,![]() 和
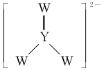
和![]() 的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将
的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将![]() 、
、![]() 转化为重要的化工原料。
转化为重要的化工原料。
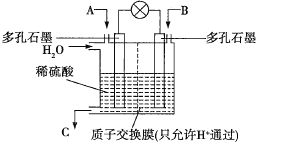
(1)若A为![]() ,B为
,B为![]() ,C为
,C为![]() ,电池总反应方程式为
,电池总反应方程式为![]() ,则正极的电极反应式为________。
,则正极的电极反应式为________。
(2)若A为![]() ,B为
,B为![]() ,C为
,C为![]() ,则负极的电极反应式为_________,电池的总反应方程式为___________。
,则负极的电极反应式为_________,电池的总反应方程式为___________。
【答案】![]()
![]()
![]()
【解析】
根据原电池工作原理进行分析解答。燃料电池的燃料做负极发生氧化反应,氧气做正极发生还原反应,注意电解质溶液对电极反应式的影响。
(1)![]() 在负极失去电子,酸性条件下该电池负极的电极反应式为
在负极失去电子,酸性条件下该电池负极的电极反应式为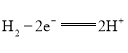 ;
;![]() 在正极得到电子,一分子
在正极得到电子,一分子![]() 得到6个电子,转化为
得到6个电子,转化为![]() ,故可得正极的电极反应式为
,故可得正极的电极反应式为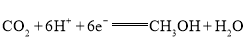 ,故答案:
,故答案: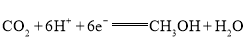 ;
;
(2)SO2在负极失去电子,可得负极的电极反应式为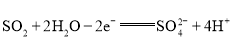 。
。![]() 在正极获得电子,可得正极的电极反应式为
在正极获得电子,可得正极的电极反应式为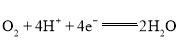 ,使正、负极得失电子总数相等并将正、负极电极反应式相加,可得电池的总反应方程式为
,使正、负极得失电子总数相等并将正、负极电极反应式相加,可得电池的总反应方程式为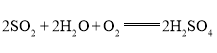 ,故答案:
,故答案: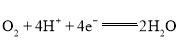 ;
;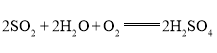 。
。

练习册系列答案
相关题目
【题目】在如图装置中,烧瓶中充满干燥气体a。将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶。a和b可能是( )
a(干燥气体) |
| |
① | NH3 | 水 |
② | CO2 | 饱和NaOH溶液 |
③ | Cl2 | 饱和食盐水 |
④ | NO2 | 水 |
⑤ | HCl | 0.1 mol·L1AgNO3溶液 |
A. ①②③B. ①②⑤C. ②④⑤D. ①②④