题目内容
【题目】下列热化学方程式或说法正确的是
A. 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
B. 已知H2(g)+F2(g)=2HF(g)△H=-270kJ·mol-1,则1molH2与1molF2反应生成2mol液态氟化氢时放热大于270kJ
C. 甲烷的标准燃烧热为△H=-890.3kJ·mol-1,则其燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ·mol-1
D. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3,放热19.3kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g)△H=-38.6kJ·mol-1
2NH3(g)△H=-38.6kJ·mol-1
【答案】B
【解析】
A.同温同压下,反应的焓变与反应条件无关,所以反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的焓变是相同的,A项错误;
B.题给热化学方程式表明1molH2和1molF2生成气态2molHF时放热270kJ,所以当生成液态氟化氢时会进一步放出热量,所以放热大于270kJ,B项正确;
C.标准燃烧热对应的水应为液态,C项错误;
D.因反应可逆,从所给数据中无法明确反应的焓变,D项错误;
答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】某小组用实验1验证FeCl3与Cu的反应,观察到有白色沉淀产生,决定对其进行深入探究。
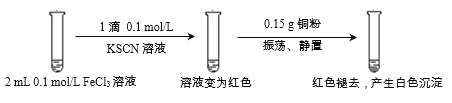
实验1:
资料:
i. CuSCN、CuCl均为难溶于水的白色固体;均能与硝酸反应,分别生成Cu2+与SO42-、Cu2+与Cl-。
ii. SCN-被称为拟卤素离子,性质与卤素离子相似;(SCN)2性质与卤素单质相似,其水溶液呈黄色。
(1)FeCl3溶液与KSCN溶液反应的离子方程式为__________________。
(2)下列由实验1得到的推论中,合理的是_______________(填字母序号)。
a. Cu能还原Fe3+
b. Fe3+与SCN-的反应是可逆反应
c. 白色沉淀中的Cu(I)(I表示+1价铜元素)可能是由Fe3+氧化Cu得到的
(3)为探究实验1中白色沉淀的成分,小组同学实施了实验2:
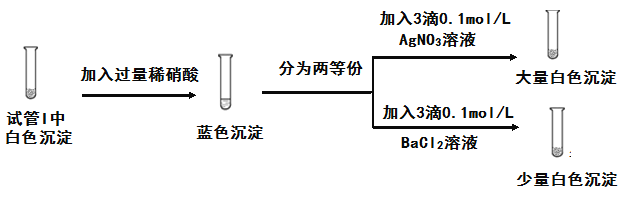
由实验2可知,实验1中白色沉淀的成分是____。
(4)该小组欲进一步探究实验1中白色沉淀产生的原因,实施了实验3:
步骤 | 实验操作 | 实验现象 |
I | 溶液变为蓝色,澄清透明,底部只有少量红色固体剩余 | |
II | 取I中上层清液于试管中,滴加1滴 0.1mol/L KSCN溶液 | 立刻出现红色,同时有白色沉淀生成 |
III | 振荡II中试管,静置 | 白色沉淀变多,红色逐渐褪去 |
①步骤I的实验操作是_____________________。
②根据实验3的现象,小组同学认为Fe3+与Cu反应的氧化产物不含Cu(I),他们的判断依据是______。
③步骤II中加入KSCN溶液后出现红色的可能原因是________________。
④解释步骤III中实验现象产生的可能原因:_______________________。