题目内容
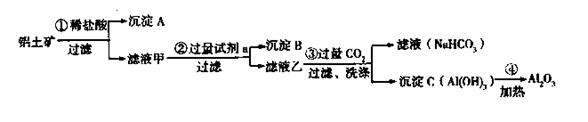
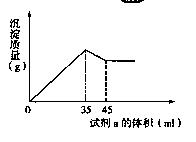
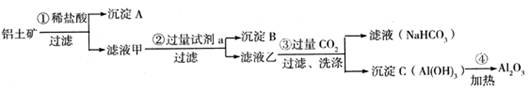
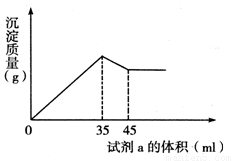
 准确称取6g铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mL 稀H2SO4溶液的烧杯中,充分反应后过滤去掉沉淀,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量和加入的NaOH溶液的体积(mL)如图所示.试回答下列问题:
准确称取6g铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mL 稀H2SO4溶液的烧杯中,充分反应后过滤去掉沉淀,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量和加入的NaOH溶液的体积(mL)如图所示.试回答下列问题:(1)当加入NaOH溶液的体积超过35mL时所发生的反应的离子方程式为
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
(2)铝土矿中Al2O3的物质的量是多少?
(3)若b=2.6,稀硫酸溶液的物质的量浓度为多少?
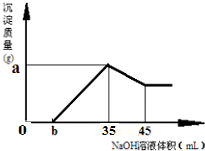
分析:(1)由图可知,加入35mL氢氧化钠溶液时,沉淀量最大,NaOH溶液的体积超过35mL时,过量的氢氧化钠与氢氧化铝反应:Al(OH)3+NaOH=NaAlO2+2H2O;
(2)从35mL~45mL加入的10mL氢氧化钠完全溶解氢氧化铝,根据n=cV计算该阶段消耗的n(NaOH),再根据方程式计算氢氧化铝的物质的量,利用铝元素守恒计算n(Al2O3);
(3)加入35mL氢氧化钠溶液时,沉淀量最大,此时溶液中溶质为硫酸钠,根据钠离子守恒计算硫酸钠的物质的量,再根据硫酸根守恒计算原硫酸溶液中n(H2SO4),再根据c=
计算.
(2)从35mL~45mL加入的10mL氢氧化钠完全溶解氢氧化铝,根据n=cV计算该阶段消耗的n(NaOH),再根据方程式计算氢氧化铝的物质的量,利用铝元素守恒计算n(Al2O3);
(3)加入35mL氢氧化钠溶液时,沉淀量最大,此时溶液中溶质为硫酸钠,根据钠离子守恒计算硫酸钠的物质的量,再根据硫酸根守恒计算原硫酸溶液中n(H2SO4),再根据c=
| n |
| V |
解答:解:(1)由图可知,加入35mL氢氧化钠溶液时,沉淀量最大,NaOH溶液的体积超过35mL时,过量的氢氧化钠与氢氧化铝反应:Al(OH)3+NaOH=NaAlO2+2H2O,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)从35mL~45mL加入的10mL氢氧化钠完全溶解氢氧化铝,该阶段消耗的n(NaOH)=0.01L×10mol/L=0.1mol,根据方程式Al(OH)3+NaOH=NaAlO2+2H2O可知,氢氧化铝的物质的量为0.1mol,根据铝元素守恒可知n(Al2O3)=0.1mol×
=0.05mol,
答:铝土矿中Al2O3的物质的量为0.05mol;
(3)当加入NaOH溶液的体积为35ml时,n(NaOH)=0.035L×10mol/L=0.35mol,
此时沉淀的质量达到最大值,则此时溶液的溶质只有Na2SO4,
根据Na元素守恒有n(Na2SO4)=
n(NaOH)=
×0.35mol=0.175mol,
根据硫酸根守恒,则有:n(H2SO4)=0.175mol,
所以原硫酸溶液中c(H2SO4)=
=1.75mol/L,
答:稀硫酸溶液的物质的量浓度为1.75mol/L.
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)从35mL~45mL加入的10mL氢氧化钠完全溶解氢氧化铝,该阶段消耗的n(NaOH)=0.01L×10mol/L=0.1mol,根据方程式Al(OH)3+NaOH=NaAlO2+2H2O可知,氢氧化铝的物质的量为0.1mol,根据铝元素守恒可知n(Al2O3)=0.1mol×
| 1 |
| 2 |
答:铝土矿中Al2O3的物质的量为0.05mol;
(3)当加入NaOH溶液的体积为35ml时,n(NaOH)=0.035L×10mol/L=0.35mol,
此时沉淀的质量达到最大值,则此时溶液的溶质只有Na2SO4,
根据Na元素守恒有n(Na2SO4)=
| 1 |
| 2 |
| 1 |
| 2 |
根据硫酸根守恒,则有:n(H2SO4)=0.175mol,
所以原硫酸溶液中c(H2SO4)=
| 0.175mol |
| 0.1L |
答:稀硫酸溶液的物质的量浓度为1.75mol/L.
点评:本题考查混合物的有关计算,难度中等,清楚图象中各阶段发生的反应是关键,注意根据守恒的计算,(3)中注意利用反应判断沉淀最大值时,溶液中的溶质,再利用守恒计算,可以简化计算过程.

练习册系列答案
相关题目
 (1)现有含Fe2O380%的赤铁矿100t,理论上可冶炼含Fe95%的生铁多少吨?
(1)现有含Fe2O380%的赤铁矿100t,理论上可冶炼含Fe95%的生铁多少吨?