题目内容
20.下列有关设计的方案能达到实验目的是( )| A. | 制备Fe(OH)3胶体:向0.1mol•L-1FeCl3溶液中加入等体积0.3mol•L-1NaOH溶液 | |
| B. | 除去FeCl3溶液中少量Cu2+:向含有少量Cu2+的FeCl3溶液中加入适量铁粉,充分反应后过滤 | |
| C. | 比较Fe(OH)3和Al(OH)3的溶度积:向0.1mol•L-1FeCl3溶液中滴加0.1 mol•L-1氨水至不再产生沉淀,然后再滴入0.1mol•L-1AlCl3溶液,观察现象 | |
| D. | 验证氧化性Fe3+<Br2<Cl2:向试管中依次加入1mL 0.1mol•L-1FeBr2溶液、几滴KSCN溶液和1mL苯,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,观察整个过程中有机相和水相中的现象 |
分析 A.氯化铁和NaOH反应生成氢氧化铁沉淀;
B.除杂时要除去杂质且不引进新的杂质;
C.溶度积大的物质能转化为溶度积小的物质;
D.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性.
解答 解:A.氯化铁和NaOH反应生成氢氧化铁沉淀,氢氧化铁胶体制备方法为:沸水中滴加几滴FeCl3饱和溶液,当加热至液体呈红褐色即为胶体,故A错误;
B.除杂时要除去杂质且不引进新的杂质,铁能和铜离子、铁离子都反应,所以不能用Fe除去氯化铁中的铜离子,故B错误;
C.比较Fe(OH)3和Al(OH)3的溶度积:向0.1mol•L-1FeCl3溶液中滴加0.1 mol•L-1氨水至不再产生沉淀时铁离子完全反应生成氢氧化铁沉淀,然后再滴入0.1mol•L-1AlCl3溶液,如果红褐色沉淀转化为白色沉淀,就说明氢氧化铁溶度积大于氢氧化铝,否则小于氢氧化铝,可以根据沉淀颜色确定溶度积大小,故C正确;
D.验证氧化性Fe3+<Br2<Cl2:向试管中依次加入1mL 0.1mol•L-1FeBr2溶液、几滴KSCN溶液和1mL苯,苯和水不互溶,二者分层且水在下层苯在上层,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,氯水氧化亚铁离子生成铁离子而导致水层呈黄色,氯气氧化溴离子生成溴单质,溴单质易溶于苯而使苯层呈橙色,观察整个过程中有机相和水相中的现象,并根据颜色变化先后顺序确定氧化性强弱,故D正确;
故选CD.
点评 本题考查化学实验方案评价,为高频考点,明确实验原理及物质性质是解本题关键,涉及氧化性强弱判断、溶度积大小比较、胶体制备、除杂等知识点,能从实验操作规范性及实验评价性分析判断,易错选项是D.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
10.苯甲酸甲酯是一种重要的工业原料,某研究性学习小组的同学拟用如图所示装置(图A中的加热装置没有画出)制取高纯度的苯甲酸甲酯,实验前他们从有关化学手册中查得相关物质的物理性质如表所示:
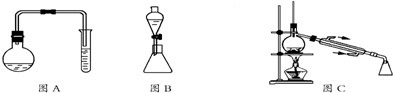
实验一:制取苯甲酸甲酯
(1)在烧瓶中混合有机物及浓硫酸的方法是先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸,试管中盛放的液体可能是Na2CO3溶液,烧瓶中反应的方程式为 .
.
实验二:提纯苯甲酸甲酯
(2)停止加热,待烧瓶内的混合物冷却后,将试管及烧瓶中的液体转移到分液漏斗中,然后塞上分液漏斗的塞子再振荡后静置,取下塞子、打开活塞,使(填主要成分的名称)苯甲酸甲酯进入锥形瓶,此时目标产物中所含杂质量最多的物质是甲醇.
(3)用图C装置进行蒸馏提纯时,当温度计显示199.6℃时,可用锥形瓶收集苯甲酸甲酯.
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g•cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

实验一:制取苯甲酸甲酯
(1)在烧瓶中混合有机物及浓硫酸的方法是先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸,试管中盛放的液体可能是Na2CO3溶液,烧瓶中反应的方程式为
 .
.实验二:提纯苯甲酸甲酯
(2)停止加热,待烧瓶内的混合物冷却后,将试管及烧瓶中的液体转移到分液漏斗中,然后塞上分液漏斗的塞子再振荡后静置,取下塞子、打开活塞,使(填主要成分的名称)苯甲酸甲酯进入锥形瓶,此时目标产物中所含杂质量最多的物质是甲醇.
(3)用图C装置进行蒸馏提纯时,当温度计显示199.6℃时,可用锥形瓶收集苯甲酸甲酯.
11.下列离子方程式的书写中,正确的是( )
| A. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 碳酸氢钠溶液跟盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| C. | 过量二氧化碳跟苛性钾反应:CO2+2OH-=CO32-+H2O | |
| D. | 硫酸氢钾和氢氧化钡按等物质的量在溶液中反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
15.短周期主族元素X、Y、Z、W原子序数依次增大,X-与氦原子电子层结构相同,Y原子核外L层电子数为8且Y与X同主族,Z原子的最外层电子数是内层电子总数的一半,W的最高正价与最低负价的代数和为4,下列说法正确的是( )
| A. | 微粒半径:X<X- | |
| B. | 简单氢化物的稳定性:Z比W的强 | |
| C. | W的氧化物的水化物的酸性一定比Z的强 | |
| D. | 最外层电子数由大到小的顺序为:Z、W、Y |
9.室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$值增大 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 再加入10 mL pH=11的NaOH溶液,酸与碱恰好完全反应 |
 .
.