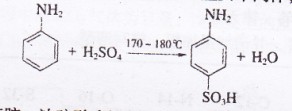
题目内容
(1)根据下列几种粒子的结构示意图,回答问题:
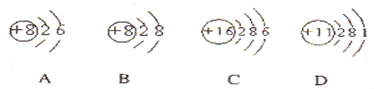
①其中属于阴离子的是
②试写出A、C、D三种元素形成的一种化合物在水溶液中的电离方程式
(2)已知氢元素有11H、12H、13H三种核素,氧元素也有816O、817O、818O三种核素,则它们所形成的水分子共有
(3)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O]
①在该反应中,氧化剂是
②当有0.20mol电子发生转移时,生成氯气的体积为
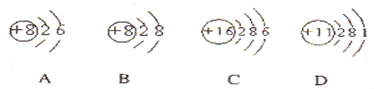
①其中属于阴离子的是
B
B
,属于金属元素的是D
D
.(填编号)②试写出A、C、D三种元素形成的一种化合物在水溶液中的电离方程式
Na2SO4═2Na++SO42-
Na2SO4═2Na++SO42-
.或Na2SO3═2Na++SO32-
或Na2SO3═2Na++SO32-
(2)已知氢元素有11H、12H、13H三种核素,氧元素也有816O、817O、818O三种核素,则它们所形成的水分子共有
18
18
种.(3)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O]
①在该反应中,氧化剂是
KMnO4
KMnO4
,还原剂是HCl
HCl
.②当有0.20mol电子发生转移时,生成氯气的体积为
2.24
2.24
L(标准状况)分析:(1)①根据示意图中所给结构示意图中质子数和核外电子数的大小关系,可以确定是原子还是离子.离子中带正电的是阳离子,带负电的是阴离子;金属元素最外层的电子数一般小于4;②根据电离方程式的书写方法来写;
(2)根据水的组成是由氢、氧元素组成,在1个水分子中含有2个氢原子和1个氧原子来分析解答;
(3)根据化合价的升降判断氧化剂、还原剂;利用电子的转移与气体的关系计算上生成的气体.
(2)根据水的组成是由氢、氧元素组成,在1个水分子中含有2个氢原子和1个氧原子来分析解答;
(3)根据化合价的升降判断氧化剂、还原剂;利用电子的转移与气体的关系计算上生成的气体.
解答:解:(1)①阴离子是质子数小于核外电子数.故B表示阴离子;金属元素原子最外层电子数少于4,故D表示金属元素,故答案为:B;D;
②A、C、D的核内质子数分别为8、16、11,所以三种元素为O、S、Na,形成的化合物为Na2SO4或Na2SO3,均为可溶性的钠盐,是强电解质,电离方程式为:Na2SO4═2Na++SO42- (或Na2SO3═2Na++SO32-),故答案为:Na2SO4═2Na++SO42- (或Na2SO3═2Na++SO32-);
(2)解:由氧的同位素有16O、17O、18O,氢的同位素有11H、12H、13H,在1个水分子中含有2个氢原子和1个氧原子,
若水分子中的氢原子相同,
则16O可分别与11H、12H、13H构成水,即存在三种水;
17O可分别与11H、12H、13H构成水,即存在三种水;
18O可分别与11H、12H、13H构成水,即存在三种水;
若水分子中的氢原子不同,
则16O可分别与11H12H、12H13H、11H13H构成水,即存在三种水;
17O可分别与11H12H、12H13H、11H13H构成水,即存在三种水;
18O可分别与11H12H、12H13H、11H13H构成水,即存在三种水;
所以共形成3×6=18种水,故答案为:18;
(3)①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,通过化合价升降判断,Mn元素由+7价降低到+2价,Cl元素的化合价由-1价升高到0,高锰酸钾得电子是氧化剂,HCl失电子是还原剂,故答案为:KMnO4;HCl;
(2)设反应中有0.20mol电子发生转移,生成氯气的体积为x,
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O 转移电子10e-,
所以电子与氯气的关系式为10e-~5Cl2
10mol 5×22.4L
0.20mol x
x=2.24L,
所以生成气体是2.24L,故答案为:2.24L.
②A、C、D的核内质子数分别为8、16、11,所以三种元素为O、S、Na,形成的化合物为Na2SO4或Na2SO3,均为可溶性的钠盐,是强电解质,电离方程式为:Na2SO4═2Na++SO42- (或Na2SO3═2Na++SO32-),故答案为:Na2SO4═2Na++SO42- (或Na2SO3═2Na++SO32-);
(2)解:由氧的同位素有16O、17O、18O,氢的同位素有11H、12H、13H,在1个水分子中含有2个氢原子和1个氧原子,
若水分子中的氢原子相同,
则16O可分别与11H、12H、13H构成水,即存在三种水;
17O可分别与11H、12H、13H构成水,即存在三种水;
18O可分别与11H、12H、13H构成水,即存在三种水;
若水分子中的氢原子不同,
则16O可分别与11H12H、12H13H、11H13H构成水,即存在三种水;
17O可分别与11H12H、12H13H、11H13H构成水,即存在三种水;
18O可分别与11H12H、12H13H、11H13H构成水,即存在三种水;
所以共形成3×6=18种水,故答案为:18;
(3)①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,通过化合价升降判断,Mn元素由+7价降低到+2价,Cl元素的化合价由-1价升高到0,高锰酸钾得电子是氧化剂,HCl失电子是还原剂,故答案为:KMnO4;HCl;
(2)设反应中有0.20mol电子发生转移,生成氯气的体积为x,
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O 转移电子10e-,
所以电子与氯气的关系式为10e-~5Cl2
10mol 5×22.4L
0.20mol x
x=2.24L,
所以生成气体是2.24L,故答案为:2.24L.
点评:本题考查的知识点较多,难度不大,需要强调的是问题(2),同位素及水的构成,明确水中的氢原子相同或不同是解答的关键,并学会利用组合的方法来分析解答即可.

练习册系列答案
相关题目
某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几种(设药片中的其他成分不与盐酸或氢氧化钠反应):
①配制0.100 mol·L-1稀盐酸和0.100 mol·L-1氢氧化钠溶液 ②取一粒药片(药片质量相同,均为0.100 g),研碎后加入20.0 mL蒸馏水 ③以酚酞为指示剂,用0.100 mol·L-1氢氧化钠溶液滴定,用去体积为V时达到终点 ④加入25.00 mL 0.100 mol·L-1稀盐酸
请回答下列问题:
(1)测定过程的正确操作顺序为:______________(填序号)。
(2)测定过程中发生反应的离子方程式为:____________________________________。
(3)若某次实验需重复测定4次。实验室现有50 mL、100 mL、250 mL、500 mL四种规格的容量瓶,则配制稀盐酸应选用的容量瓶规格最好为___________ ,理由是____________________________________。
(4)某同学四次测定的V数据如下:
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
V/mL | 12.9 | 15.4 | 13.1 | 13.0 |
请根据这位同学的实验数据,计算药片中碳酸钙的质量分数。
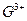 离子与Ar原子的电子层结构相同。请回答:
离子与Ar原子的电子层结构相同。请回答: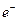 。的稳定结构
。的稳定结构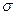 键 h.
键 h.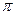 键
键
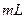 ,冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出。用该烧杯中的少量冷水将a内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到粗产品。
,冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出。用该烧杯中的少量冷水将a内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到粗产品。 是 。
是 。