题目内容
【题目】某制药厂利用C2H4、水杨酸以及C4H8合成一种药物K,其合成路线设计如下:
| |
D能与NaHCO3溶液作用生成气体,遇FeCl3溶液不显紫色;G无酸性,H、I有酸性。
(1)上述过程中属于取代反应的是_____________________;
(2)C结构中官能团的电子式为_______________,E的结构简式为__________________________;
(3)反应⑦的化学方程式为______________________________________________;
(4)D与足量NaOH溶液共热的化学方程式为_________________________________________________________;
(5)I的属于链状酯类化合物的同分异构体共有_________种(不考虑立体异构)。
【答案】 ②③⑤⑧ ![]() CH2=C(CH3)2 HOC(CH3)2COOH
CH2=C(CH3)2 HOC(CH3)2COOH ![]() CH2=C(CH3)COOH + H2O
CH2=C(CH3)COOH + H2O ![]() 5
5
【解析】A是乙烯,与溴水发生加成反应B,B为1,2-二溴乙烷,1,2-二溴乙烷在氢氧化钠水溶液中发生水解反应生成C,C为乙二醇。D可与NaHCO3溶液作用生成气体,遇FeCl3溶液不显紫色,说明D含有酯基和羧基,不含酚羟基,所以D的结构简式为![]() ;E(C4H8)与溴水发生加成反应生成F,F为二溴代丁烷,2个溴原子处于相邻碳原子上,F水解生成G,G氧化生成H,H在浓硫酸、加热条件下生成I,G无酸性,H、I有酸性,则H、I含有-COOH,则H发生消去反应生成I,故H中含有-OH、-COOH,连接同一碳原子上,连接醇羟基的碳原子上没有氢原子,故H为
;E(C4H8)与溴水发生加成反应生成F,F为二溴代丁烷,2个溴原子处于相邻碳原子上,F水解生成G,G氧化生成H,H在浓硫酸、加热条件下生成I,G无酸性,H、I有酸性,则H、I含有-COOH,则H发生消去反应生成I,故H中含有-OH、-COOH,连接同一碳原子上,连接醇羟基的碳原子上没有氢原子,故H为 ,I为
,I为 ,逆推可得,G的结构简式为:HOCH2COH(CH3)2,F为BrCH2CBr(CH3)2,E为CH2=C(CH3)2。C、D、I一定条件下生成J,J加聚反应生成K,结合K的结构简式可知,J的分子式为C15H16O6,生成J的反应为酯化反应,J为
,逆推可得,G的结构简式为:HOCH2COH(CH3)2,F为BrCH2CBr(CH3)2,E为CH2=C(CH3)2。C、D、I一定条件下生成J,J加聚反应生成K,结合K的结构简式可知,J的分子式为C15H16O6,生成J的反应为酯化反应,J为 。
。
(1)根据以上分析可知上述过程中属于取代反应的是②③⑤⑧;(2)C结构中官能团是羟基,电子式为![]() ,E的结构简式为CH2=C(CH3)2;(3)反应⑦的化学方程式为HOC(CH3)2COOH
,E的结构简式为CH2=C(CH3)2;(3)反应⑦的化学方程式为HOC(CH3)2COOH ![]() CH2=C(CH3)COOH + H2O;(4)D与足量NaOH溶液共热的化学方程式为
CH2=C(CH3)COOH + H2O;(4)D与足量NaOH溶液共热的化学方程式为![]() ;(5) I的属于链状酯类化合物的同分异构体为HCOOCH2CH=CH3、HCOOCH2CH=CH2、HCOOC(CH3)=CH2、CH3COOCH=CH2、CH2=CHCOOCH3,共有5种(不考虑立体异构)。
;(5) I的属于链状酯类化合物的同分异构体为HCOOCH2CH=CH3、HCOOCH2CH=CH2、HCOOC(CH3)=CH2、CH3COOCH=CH2、CH2=CHCOOCH3,共有5种(不考虑立体异构)。

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】汽车尾气中含有上百种化合物,污染物中以NO为主。请回答下列与NO相关的问题:
(1)汽车发动机工作时燃料燃烧会使氮气转化为NO。
已知:N2(g)+O2(g)=2NO(g) △H=+akJ·mol-1。NO中氮氧键键能为b kJ·mol-1、O=O键能为 c kJ·mol-1。
计算N_N的键能为____________kJ·mol-1(用含a、b、c的代数式表示)。
(2)NO和CO在一定温度和催化剂的条件下可发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-538 kJ·mol-1。
N2(g)+2CO2(g) △H=-538 kJ·mol-1。
一定温度下,向体积为2L的密闭容器中充入一定量的NO和CO,发生上述反应。反应过程中测定的部分数据见下表:
时间/min | n(NO)/mol | n(CO)/mol | n(N2)/mol | n(CO2)/mol |
0 | 0.100 | 0.200 | 0 | 0 |
4 | 0.020 | |||
6 | 0.050 | |||
8 | 0.025 |
①反应在0~4 min内的平均速率v(CO)=_____________。
②下列叙述中,能说明反应已达到平衡的是____________。
a.NO的消耗速率和CO2的生成速率相等 b.容器内的压强不再变化
c.混合气体的密度不再变化 d.N2的百分含量不再变化
③计算该温度下的平衝常数K=____________。
④8min时,其他条件不变,向该反应容器中再通入0.05molNO和0.100CO,重新达到平衡时混合气体中N2的百分含量将____________(填“减小”、“增大”或“不变” )。
(3)工业上采用电解NO的方法制备NH4NO3,其工作原理如图。X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充NH3。
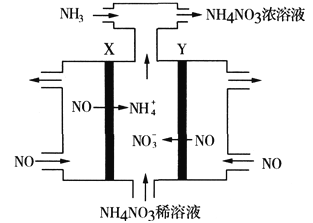
①Y电极上的电极反应式为_______________________________。
②若X电极上有11.2L(已换算成标准状况)NO发生反应,则生成NH4NO3的质量为____________g。





