题目内容
X、Y是原子序数大于4的两种主族元素,它们的离子Xm+ 和Yn- 具有相同的核外电子排布。有关X、Y的叙述不正确的是( )
| A.原子序数大小:X>Y |
| B.Xm+和Yn-离子半径大小:Yn-<Xm+ |
| C.在周期表中X、Y在不同周期 |
| D.在周期表中X、Y的族序数之差为:8-(m+n) |
B
解析试题分析:由题意可知Xm+ 和Yn- 具有相同的核外电子排布,则具有相同的核外电子数,X失去m个电子与Y得到n个电子后具有相同的核外电子数,确定原子序数X>Y,且两者不在同周期,则A、C正确;D项:分析可知X的族序数为m,Y的族序数为8-n,两者族序数之差为8-(m+n),正确;B项错误:因为具有相同的核外电子排布的离子,原子序数越大离子半径越小。所以离子半径应为Yn- >Xm+
考点:元素周期表的知识以及微粒半径大小的比较。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于 、
、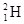 、
、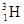 的说法正确的是( )
的说法正确的是( )
| A.它们的中子数相同 | B.它们是相同的原子 |
| C.它们的性质相似 | D.它们是氢元素的三种同位素 |
依据元素周期表及元素周期律,下列推断正确的是
| A.同一周期元素的原子,半径越小越容易失去电子 |
| B.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| C.若M+和R2-的核外电子层结构相同,则原子序数R>M |
| D.主族元素的最高正化合价等于该元素原子的最外层电子数 |
下列分子中所有原子都满足最外层为8个电子结构的是 ( )
| A.BF3 | B.H2O | C.SiCl4 | D.PCl5 |
某元素X的逐级电离能如图所示,下列说法正确的是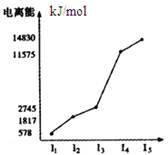
| A.X元素显+4价 |
| B.X为非金属 |
| C.X为第五周期元素 |
| D.X与氯反应时最可能生成的阳离子为X3+ |
以下能级符号不正确的是
| A.2d | B.3s | C.4p | D.5f |
下列分子中所有原子都满足最外层8电子结构的是
| A.光气(COCl2) | B.六氟化硫 | C.二氟化氙 | D.三氟化硼 |
下列说法正确的是
| A.电子层结构相同的微粒,其化学性质一定相似 |
| B.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C.非金属元素的原子两两结合形成的化合物不一定是共价化合物 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
元素性质的周期性变化不包括
| A.原子半径 | B.元素的主要化合价 |
| C.原子核外电子结构 | D.金属性和非金属性 |