��Ŀ����
9�����Ȼ�������ýȾ�����л��ϳ��ϵ��Ȼ�������ʵ�����Ʊ����Ȼ����ķ�Ӧ��װ��ʾ��ͼ���й���Ϣ�������£�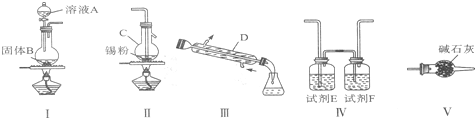
�й���Ϣ���ݣ��ٽ����������ڣ�ͨ������������з�Ӧ���������Ȼ���������ˮ���Ȼ�������ɫ��������Һ�壬�۵�-33�棬�е�114.1�森����ˮ���Ȼ�����¶�ڿ�����������е�ˮ�ַ�Ӧ���ɰ�ɫ��������ǿ�ҵĴ̼��ԣ��ش��������⣺
��1������C��������������ƿ������D�������ǽ�SnCl4��������ΪҺ�壮
��2���Ʊ���ˮ���Ȼ�����װ�õ�����˳���Ǣ�һ��һ��һ��һ�� ����װ����ţ���
��3���Լ�E��F�ֱ��DZ���ʳ��ˮ��Ũ���ᣬװ��V������������δ��Ӧ����������ֹ�����е�ˮ��������װ�â��ڣ�ʹSnCl4ˮ�⣻��
��4������װ��V���ڣ���װ�â��г�����SnCl4�⣬�����ڵĸ�����Ļ�ѧʽΪSn��OH��4��SnO2
��5��ʵ���Ƶõ�SnCl4�����ܽ���C12�����Ի�ɫ���ᴿSnCl4�ķ����Ǽ�������
��6����������ȥ����5.95g����Ӧ������ƿ���ռ���12.0g SnCl4����SnCl4�IJ���Ϊ92.0%�����������λ��Ч���֣���
���� ��װ��ͼ��֪װ�â�ӦΪ�Ʊ�����װ�ã����ӷ�ӦΪ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��װ��EΪ����ʳ��ˮ��װ��FΪŨ���ᣬ���������ӣ������������װ�â��з�Ӧ����SnCl4������ȴ����װ�â����ռ�����SnCl4����ˮ�⣬Ӧ��ֹ�����е�ˮ��������װ�â��У�ͨ������װ��V��ʵ�֣��Դ˽����⣮
��� �⣺��1����װ��ͼ��֪����CΪ������ƿ������D�������ǽ�SnCl4��������ΪҺ�壬�Ӷ��ռ�������
�ʴ�Ϊ��������ƿ����SnCl4��������ΪҺ�壻
��2����ʵ�������Ʊ����������������ӣ������������װ�â��з�Ӧ����SnCl4������ȴ����װ�â����ռ�����SnCl4����ˮ�⣬Ӧ��ֹ�����е�ˮ��������װ�â��У���������˳����I������������V��
�ʴ�Ϊ��I��������V��
��3��װ�â�����ֵ�õ������к����Ȼ����ˮ������װ��EΪ����ʳ��ˮ����ȥ�Ȼ��⣬װ��FΪŨ���ᣬ��ȥˮ��������SnCl4����ˮ�⣬Ӧ��ֹ�����е�ˮ��������װ�â��У�ͨ������װ��V��ʵ�֣�
�ʴ�Ϊ������ʳ��ˮ��Ũ�������δ��Ӧ����������ֹ�����е�ˮ��������װ�â��ڣ�ʹSnCl4ˮ�⣻
��4������װ��V���ڣ����������к���ˮ�����������ڢ��г�����SnCl4�⣬��������SnCl4ˮ������ĺ����Ļ�����Sn��OH��4��SnO2��
�ʴ�Ϊ��Sn��OH��4��SnO2��
��5��ʵ���Ƶõ�SnCl4�����ܽ���Cl2�����Ի�ɫ����������ķ������ӣ�
�ʴ�Ϊ����������
��6����������ȥ����5.95g����n��Sn��=$\frac{5.95g}{119g/mol}$=0.05mol�������ϲ�����SnCl4�����ʵ�������m��SnCl4��=0.05mol��261g/mol=13.05g�����Է�Ӧ������ƿ���ռ���12.0gSnCl4����SnCl4�IJ���Ϊ$\frac{12.0g}{13.05g}$��100%=92.0%���ʴ�Ϊ��92.0%��
���� ���⿼�����ʵ��Ʊ����漰������ʶ��������ʵ������ȡ������ʵ�������Ŀ�ġ�����ˮ�⡢���ʲ��ʵļ����֪ʶ��������ѧ���ķ���������ʵ�������Ŀ��飬ע����������Ϣ��������ʵ��������ʵ�鲽�裬��Ŀ�ѶȲ���

 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
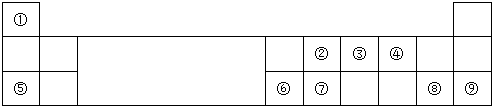
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
��2��������������ˮ�����У�������ǿ�Ļ�����ķ���ʽ��HClO4��������ǿ�Ļ�����ĵ���ʽ��
 ��
����3���õ���ʽ��ʾԪ�آ���Ļ�������γɹ��̣�
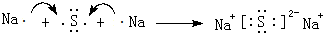 ���û������������ӣ�����ۡ������ӡ��������
���û������������ӣ�����ۡ������ӡ����������4���ۡ��ޡ�������Ԫ���γɵ����ӣ����Ӱ뾶�ɴ�С��˳����S 2-��Cl-��O2-�������ӷ��ű�ʾ����
��5��Ԫ�آ۵��⻯��ĽṹʽΪH-O-H�����⻯�ﳣ���º�Ԫ�آߵĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪCl2+H2O=HCl+HClO��
| ����� | �Լ� | ���뷽�� | |
| �� | �屽��Br2�� | NaOH��Һ | ��Һ |
| �� | ���飨��ϩ�� | ��ˮ | ϴ�� |
| �� | ��Ȳ��H2S�� | ����ͭ��Һ | ϴ�� |
| �� | ��ϩ��SO2�� | NaOH��Һ | ϴ�� |
| �� | CO2��HCl�� | ����̼��������Һ | ϴ�� |
| A�� | KClO3 ��SO3 ����ˮ���ܵ��磬��KClO3��SO3Ϊ����� | |
| B�� | 25��ʱ���ô�����Һ�ζ���Ũ��NaOH ��Һ��pH=7��V������VNaOH | |
| C�� | ��NaAlO2 ��Һ�еμ�NaHCO3 ��Һ���г������������� | |
| D�� | AgCl ��ת��ΪAgI ������K��AgX��=c��Ag+ ��•c��X-������K��AgI����K��AgCl�� |
| A�� | ҽ�þƾ���ָ��������Ϊ75%���Ҵ���Һ | |
| B�� | �ù��˵ķ������Է����Ҵ����������� | |
| C�� | ������ȥ�۵�ԭ����������ˮ��Һ���ܵ���������ӣ���ˮ���ţ���Ӳ֬������ӣ����ͻ��ţ��������ǵĹ�ͬ�����£�ͨ����ϴ�����·��ϵ����ۡ�����ˮ�� | |
| D�� | �����ǡ���������һ�������¶��ܷ���������Ӧ |
| A�� | S��Cl | B�� | Na��K | C�� | N��O | D�� | F��Mg |
 ��
��