题目内容
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HA![]() H++A-,回答下列问题:
H++A-,回答下列问题:
(1)若向溶液中加入少量Na,以上平衡将向________(填“正”、“逆”)反应方向移动,溶液中c(OH-)将________(填“增大”、“减小”或“不变”)。
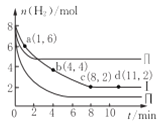
(2)在一定温度下,HA加水稀释过程中溶液的导电能力如右图所示,请回答:

①a、b、c三点溶液中,c(H+)由小到大的顺序是: 。
②a、b、c三点溶液中,HA的电离程度最大的是: 。
(3)在25℃下,将c mol/L的HA与0.01mol/L的NaOH溶液等体积混合,反应平衡时溶液中c(Na+)=c(A-)。请用含c的代数式表示HA的电离常数Ka=________(注明单位)。
【答案】(1)正 增大 (2)a﹤c﹤b;c(3)![]() mol/L
mol/L
【解析】
试题分析:(1)若向溶液中加入少量Na,Na和H+发生反应,H+浓度减小,平衡将向正反应方向移动,温度不变,Kw不变,溶液中c(OH-)将增大。
(2)①溶液的导电能力越强,溶液中自由移动离子浓度越大,根据图像知a、b、c三点溶液中,c(H+)由小到大的顺序是a﹤c﹤b;②加水稀释促进弱电解质的电离,根据图像知a、b、c三点溶液中,HA的电离程度最大的是c。
(3)溶液的电荷守恒式为c(H+)+ c(Na+)=c(A-)+c(OH-),反应平衡时溶液中c(Na+)=c(A-),则c(H+)=c(OH-)=10-7mol/L,电离常数只与温度有关,此时HA的电离常数Ka= c(H+) c(A-)/c(HA) =(0.005mol/L×10-7mol/L)÷(a/2-0.005mol/L)= ![]() mol/L。
mol/L。

练习册系列答案
相关题目