题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使甲基橙呈红色的溶液中:K+、AlO2-、NO3-、CO32-
B.c(ClO-)=1.0mol/L的溶液:Na+、SO32-、S2-、Cl-
C.水电离出来的c(H+)=l×l0-12mol/L的溶液:K+、NH4+、SO42-、Fe3+
D.![]() 的溶液:Na+、AlO2-、CO32-、NO3-
的溶液:Na+、AlO2-、CO32-、NO3-
【答案】D
【解析】
试题分析:A.使甲基橙呈红色的溶液显酸性,AlO2-和CO32-均不能大量共存,A错误;B.c(ClO-) = 1.0 mol /L的溶液中SO32-、S2-易被氧化而不能大量共存,B错误;C.水电离出来的 c(H+) = l×l0-12mol/L的溶液中水的电离被抑制,溶液可能显酸性,也可能显碱性,如果显碱性NH4+和Fe3+均不能大量共存,C错误;D.![]() 的溶液中氢氧根浓度是0.1mol/L,溶液显碱性,因此Na+、AlO2-、CO32-、NO3-均可以大量共存,D正确,答案选D。
的溶液中氢氧根浓度是0.1mol/L,溶液显碱性,因此Na+、AlO2-、CO32-、NO3-均可以大量共存,D正确,答案选D。

 阅读快车系列答案
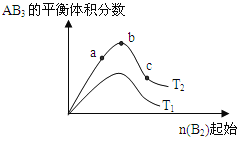
阅读快车系列答案【题目】在自来水消毒和工业上砂糖、油脂的漂白与杀菌过程中,亚氯酸钠(NaClO2)发挥着重要的作用。下图是生产亚氯酸钠的工艺流程图:
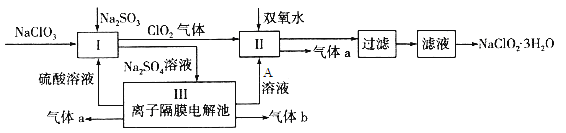
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;
②常温下,Ksp(FeS)=6.3×10-18;Ksp(CuS)=6.3×10-36;Ksp(PbS)=8×10-28
③Ⅲ装置中电解硫酸钠溶液,阳极区生成氧气同时产生硫酸,阴极区生成氢气同时产生氢氧化钠。
(1) I中发生反应的离子方程式为 ____________。
(2)从滤液中得到NaClO2·3H2O晶体的所需操作依次是 (填写序号)。
a.蒸馏 b.蒸发浓缩 c.过滤 d.冷却结晶 e.灼烧
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。下表是25℃时HClO2及几种常见弱酸的电离平衡常数:
弱酸 | HClO2 | HF | H2CO3 | H2S |
Ka/mol·L-1 | 1×10-2 | 6.3×10-4 | K1=4.30×10-7 K2=5.60×10-11 | K1=9.1×10-8 K2=l.1×10-12 |
①常温下,物质的量浓度相等的NaClO2、NaF、NaHCO3、Na2S四种溶液的pH由大到小的顺序为 (用化学式表示);
②Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是 ;常温下,当最后一种离子沉淀完全时(该离子浓度为10-5mol·L-1)此时体系中的S2-的浓度为 。
(4)Ⅲ装置中若生成气体a的体积为1.12L(标准状况),则转移电子的物质的量为________。
【题目】下列各组物质中,不能按图示(“→”表示一步完成)关系相互转化的是
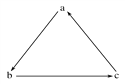
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | H2SO4 | SO2 | SO3 |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A. A B. B C. C D. D