题目内容
【题目】下图装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:

(1)c极的电极反应式为_________。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,电解进行一段时间后,你能观察到的现象是:___________, 电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应式为_____________。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了____moL气体,此时若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为_________。此时A池中溶液pH为_________。(假设电解前后A池溶液体积无变化,数据化成最简形式即可)
【答案】 2I—-2e-=I2 C极附近溶液变为蓝色 4OH——4e-=2H2O+O2 0.001 108g/mol 2-lg2
【解析】由电解原理可得:金属M沉积于b极,说明b是阴极,则a是阳极,c是阳极,d是阴极,(1)因c是阳极,溶液中的阴离子放电,根据离子的放电顺序,可知是2I--2e-=I2;(2)在B烧杯中, c是阳极,溶液中的阴离子放电,即2I--2e-=I2,I2遇到淀粉能使淀粉变蓝,电解进行一段时间后,I-放电完毕后,接着是OH-放电,罩在c极上的试管中也收集到了气体,此时c极上的电极反应式为:4OH--4e-=2H2O+O2↑;(3)d电极上收集的44.8ml气体(标准状况)是氢气,a极上收集到的气体是氧气,根据转移电子数相等知,氧气和氢气的体积之比是1:2,d电极上收集的44.8ml气体氢气,则a电极上收集到22.4mL氧气;物质的量为0.001mol,d电极上析出的氢气的物质的量=![]() =0.002mol,转移电子的物质的量是0.004mol,硝酸盐中M显+1价,所以当转移0.004mol电子时析出0.004mol金属单质,M=
=0.002mol,转移电子的物质的量是0.004mol,硝酸盐中M显+1价,所以当转移0.004mol电子时析出0.004mol金属单质,M=![]() =108g/mol; A池中a是阳极,阳极上氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,根据转移电子数相等知,转移电子的物质的量是0.004mol,则产生的氢离子的物质的量为0.004mol,c(H+)=
=108g/mol; A池中a是阳极,阳极上氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,根据转移电子数相等知,转移电子的物质的量是0.004mol,则产生的氢离子的物质的量为0.004mol,c(H+)=![]() =2.0×10-3mol/L,pH=- lg c(H+)=2-lg2。
=2.0×10-3mol/L,pH=- lg c(H+)=2-lg2。

 课时训练江苏人民出版社系列答案
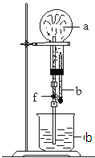
课时训练江苏人民出版社系列答案【题目】在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.a和b分别是( )
a(干燥气体) | b(液体) | |
① | NO2 | 水 |
② | CO2 | 4molL-1NaOH溶液 |
③ | Cl2 | 饱和食盐水 |
④ | NH3 | l molL-1盐酸 |
A. ①和② B. ③和④ C. ①和③ D. ②和④