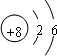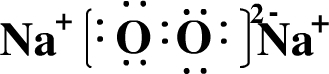题目内容
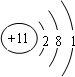
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子数总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1.试回答:
(1)写出基态D原子的电子排布式
(2)用电子式表示AE2的形成过程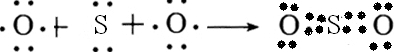
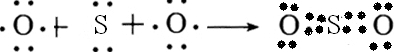 ,与AE2互为等电子体的离子是
,与AE2互为等电子体的离子是
(3)B、C两元素的第一电离能较大的元素是:
(4)根据VSEPR模型预测C的氢化物的立体结构为
(5)C的单质中π键的数目为
(1)写出基态D原子的电子排布式
1s22s22p63s23p2
1s22s22p63s23p2
.(2)用电子式表示AE2的形成过程
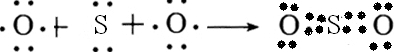
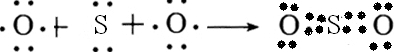
N3-(或CNO-)
N3-(或CNO-)
.(3)B、C两元素的第一电离能较大的元素是:
N
N
(填写元素符号).(4)根据VSEPR模型预测C的氢化物的立体结构为
三角锥形
三角锥形
,中心原子C的轨道杂化类型为sp3
sp3
.(5)C的单质中π键的数目为
2
2
,B、D两元素的气态氢化物的稳定性大小关系为:H2O
H2O
>SiH4
SiH4
(填写化学式).分析:p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,则A的核外电子排布为1s22s22p2,应为C元素,B原子最外层中有两个不成对的电子,核外电子排布式为1s22s22p4,为O元素,B元素可分别与A、C、D、E生成RB2型化合物,且A、B、C属于同一周期,则C为N元素,可形成NO2化合物,在DB2和EB2中,D与B的质量比为7:8,则有M(D):M(O)=7:4,M(D)=7×
=28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,结合元素对应原子的结构、单质以及化合物的性质解答该题.
| 16 |
| 4 |
解答:解:p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,则A的核外电子排布为1s22s22p2,应为C元素,B原子最外层中有两个不成对的电子,核外电子排布式为1s22s22p4,为O元素,B元素可分别与A、C、D、E生成RB2型化合物,且A、B、C属于同一周期,则C为N元素,可形成NO2化合物,在DB2和EB2中,D与B的质量比为7:8,则有M(D):M(O)=7:4,M(D)=7×
=28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,
(1)D为Si元素,原子序数为14,基态原子的核外电子排布式为1s22s22p63s23p2,
故答案为:1s22s22p63s23p2;
(2)AE2为CS2,为共价化合物,根据化合物中各原子最外层满足8电子稳定结构,可写出用电子式表示的形成过程为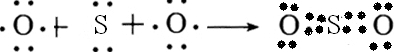 ,与CS2等电子体的离子有N3-、CNO-等,
,与CS2等电子体的离子有N3-、CNO-等,
故答案为: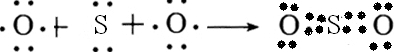 ;N3- (或CNO-);
;N3- (或CNO-);
(3)由于N原子2p轨道为半充满状态,第一电离能较大,所以第一电离能N>O,故答案为:N;
(4)NH3中,N原子与H原子形成3个δ键,孤电子对数为
=1,空间构型为三角锥形,N原子的杂化轨道类型为sp3杂化,
故答案为:三角锥形;sp3;
(5)C为N元素,形成的单质为N≡N,含有2个π键,由于O的非金属性大于Si,则稳定性:H2O>SiH4,
故答案为:2;H2O;SiH4.
| 16 |
| 4 |
(1)D为Si元素,原子序数为14,基态原子的核外电子排布式为1s22s22p63s23p2,
故答案为:1s22s22p63s23p2;
(2)AE2为CS2,为共价化合物,根据化合物中各原子最外层满足8电子稳定结构,可写出用电子式表示的形成过程为
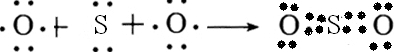 ,与CS2等电子体的离子有N3-、CNO-等,
,与CS2等电子体的离子有N3-、CNO-等,故答案为:
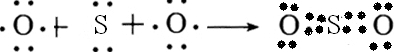 ;N3- (或CNO-);
;N3- (或CNO-);(3)由于N原子2p轨道为半充满状态,第一电离能较大,所以第一电离能N>O,故答案为:N;
(4)NH3中,N原子与H原子形成3个δ键,孤电子对数为
| 5-3×1 |
| 2 |
故答案为:三角锥形;sp3;
(5)C为N元素,形成的单质为N≡N,含有2个π键,由于O的非金属性大于Si,则稳定性:H2O>SiH4,
故答案为:2;H2O;SiH4.
点评:本题考查较为综合,涉及元素的推断、电子排布式的书写、电子式、第一电离能、杂化类型以及元素周期律等知识,题目难度中等,本题中正确推断元素的种类为解答该题的关键.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目