题目内容
(12分)400 ℃时,将一定量的SO2和 14 mol O2压入一个盛有催化剂的10 L密闭容器中进行反应:2SO2+O2 2SO3
2SO3
已知 2 min后,容器中剩余 2 mol SO2和12 mol O2。试计算:
(1)生成SO3 的物质的量。
(2)SO2的起始物质的量浓度。
(3)2 min 内SO2和SO3 的反应速率。
【答案】
2SO2 +
O2  2SO3
2SO3
起始量(mol) x 14 0
转化量(mol) 4 2 4
2min后(mol0 x-4 12 4
所以(1)生成SO3的物质的量是4mol
(2)x-4mol=2mol,所以SO2的起始物质的量是x=6mol,则SO2的起始物质的量浓度为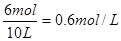 。
。
(3)反应速率通常用单位时间内浓度的变化量来表示,因为二者的浓度变化量是相同的,所以2 min 内SO2和SO3 的反应速率相同,都是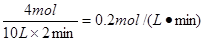 。
。
【解析】考查有关化学反应速率的计算。在有关反应速率的计算时一般采用三段式进行计算,即根据反应式分别列出起始量、转化量和平衡量(或某时刻的量),然后在根据已知条件进行列式计算。

练习册系列答案
相关题目
 2SO3
2SO3 3NH3(g) ,△H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。回答下列问题:
3NH3(g) ,△H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。回答下列问题: