题目内容
某校化学小组学生进行如下实验.
(1)使用铜和稀硫酸制备硫酸铜晶体.步骤如下∶
步骤①观察到的现象是________.步骤③的主要操作包括∶________.
(2)硫酸铜溶解度的测定.
用石墨电极(相同)电解饱和CuSO4溶液,阴极的电极反应式是________.已知饱和CuSO4溶液的质量为60 g,通电10 min后,溶液恰好变为无色.称量发现两电极质量差为4 g,此温度下CuSO4的溶解度是________.
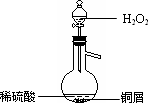
(3)某同学查询资料得知∶铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解.实验小组同学设计实验装置如图,验证该实验,该反应的化学方程式是________.若将H2O2和稀硫酸加入烧瓶中的顺序颠倒,实验得到的结论是________.
解析:
|
红色固体变黑,加热浓缩,冷却结晶,过滤;Cu2++2e-==Cu,20 g;Cu+H2O2+H2SO4=CuSO4+2H2O,铜屑放入H2O2中不发生反应,若在H2O2中加入稀硫酸,铜屑可逐渐溶解. |

气体 | A | B | C | D | E | F |
烧瓶和气体的总质量/g | 48.4082 | 48.4082 | 48.4082 | 48.3822 | 48.4342 | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.4212 g。空气的平均相对分子质量为29。A、B、C、D、E、F是中学常见的气体。
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)________________。
(2)E的相对分子质量是________。
(3)实验室制取少量D的化学方程式是______________________________。
(4)A、B、C可能的化学式是______________________________________________。
气体 | A | B | C | D | E | F |
烧瓶和气体的总质量/g | 48.4082 | 48.4082 | 48.4082 | 48.3822 | 48.4342 | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.4212 g。空气的平均相对分子质量为29。A、B、C、D、E、F是中学常见的气体。
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)________________。
(2)E的相对分子质量是_________。
(3)实验室制取少量D的化学方程式是________________________________________。
(4)A、B、C可能的化学式是________________。
某校化学小组学生进行“气体相对分子质量的测定”的实验。操作如下:用质量和容积都相等的烧瓶收集气体,称量收集满气体的烧瓶质量。数据见下表(已换算成标准状况下的数值)。?
气体 | A | B | C | D | E | F |
烧瓶和气体的总质量/g | 48.4082 | 48.408 2 | 48.4082 | 48.3822 | 48.4342 | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量是48.4212 g。空气的平均相对分子质量为29。A、B、C、D、E、F是中学常见的气体。?
(1)上述六种气体中,能够使品红溶液褪色的是(写化学式)_______________。
(2)E的相对分子质量是____________。
(3)实验室制取少量D的化学方程式是____________________________________。
(4)A、B、C可能的化学式是__________________________________________________。