��Ŀ����
��һ�ݻ�Ϊ2 L���ܱ������У�����0.2 mol��N2��0.6 mol��H2����һ�������·�����Ӧ��N2(g)��3H2(g)  2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺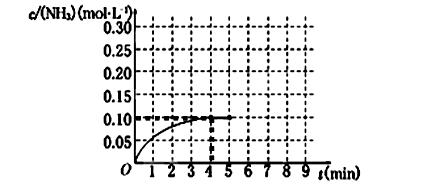
��1��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��������ƽ����Ӧ����v(H2)Ϊ______________��
��2���÷�Ӧ�ﵽƽ��ʱN2��ת����_________________��
��3����Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ____________��(�����)
a��0.20 mol��L��1 b��0.12 mol��L��1 c��0.10 mol��L��1 d��0.08 mol��L��1
��4����д���÷�Ӧ��ƽ�ⳣ������ʽ_________�����÷�Ӧ��298K��398Kʱ�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2����K1 K2�����������="��" �� ������ ����
��5���ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ��(��ʱNH3��Ũ��ԼΪ0.25 mol��L��1)��������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߡ�
��1��0.0375 mol��L��1��min��1
��2��50%
��3��a��c
��4��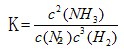 >
>
��5��
���������������1��v(H2)="3/2" v(NH3)=3/2��0.10mol/L��4min=0.0375 mol��L��1��min��1��
N2(g)��3H2(g)  2NH3(g)
2NH3(g)
��ʼŨ�ȣ�mol?L?1��0.1 0.3 0
��ʼŨ�ȣ�mol?L?1��0.05 0.15 0.1
��ʼŨ�ȣ�mol?L?1��0.05 0.15 0.1
��÷�Ӧ�ﵽƽ��ʱN2��ת����=0.05mol?L?1��0.1mol?L?1��100%=50%
��3�����ݻ�ѧ����ʽ��֪NH3��Ũ�ȷ�Χ0<c(NH3)<0.2mol?L?1��ԭƽ��NH3��Ũ��Ϊ0.10mol?L?1���¶ȸı䣬ƽ���ƶ��ᷢ���ƶ�����ƽ���Ũ��һ������0.10mol?L?1����a��c����ܡ�
��4������ƽ�ⳣ���Ķ���ɵø÷�Ӧ��ƽ�ⳣ������ʽΪ��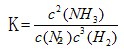 ����Ϊ����ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С������K1>K2��
����Ϊ����ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С������K1>K2��
��5����5����ĩ�������������Сһ���NH3��Ũ�ȱ�Ϊ0.20mol?L?1��ѹǿ����ƽ�������ƶ���NH3��Ũ�������ӣ���8minĩΪ0.25mol?L?1�����ɻ������ߡ�
���㣺���⿼�黯ѧ��Ӧ���ʺͻ�ѧƽ��ļ��㡢Ũ�ȷ�Χ���жϡ���ѧƽ�ⳣ����Ũ�����ߵĻ��ơ�

 ��У������Ԫͬ��ѵ��������ϵ�д�
��У������Ԫͬ��ѵ��������ϵ�д��Ѵ����е�����̬�ĵ�ת��Ϊ���Ļ�����Ĺ��̳�Ϊ�̵�������̵��ʹ����̵�������ʱN2ת��ΪNO��������Ȼ�̵�����Զ���������������Ҫ����ҵ�̵����ϳɰ�����Ŀǰ�˹��̵�����Ҫ�������йش����̵���ҵ�̵���ƽ�ⳣ��Kֵ�ֱ����±�һ�ͱ�����
��һ��N2+ O2 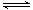 2NO
2NO
| �¶� | 27�� | 2000�� |
| Kֵ | 3��84��10��31 | 0��1 |
������N2+ 3H2
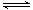 2NH3
2NH3 | �¶� | 25�� | 350�� | 400�� | 450�� |
| Kֵ | 5��108 | 1��847 | 0��507 | 0��152 |
A��N2+ O2
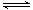 2NO�����ȷ�Ӧ
2NO�����ȷ�ӦB��������ģģ������̵���û�������
C���ڳ����£����ӹ�ҵ�̵���������ѹǿ��Kֵ�ᷢ���ı�
D����ҵ�̵��Ƿ��ȷ�Ӧ
��2����ij�ܱ������м���4 mol NH3��1��2 mol H2��һ������N2�������壬һ�������·�����Ӧ�������ʵ�Ũ����ʱ��仯���ͼ��ʾ[��֪0��t1�α��ֺ��¡����ݣ���c(N2)δ����]����ͼΪt2ʱ�̺�ı䷴Ӧ��������Ӧ������ʱ��ı仯�������֪��t2��t3��t4��t5ʱ�̸��ı�һ�ֲ�ͬ��������
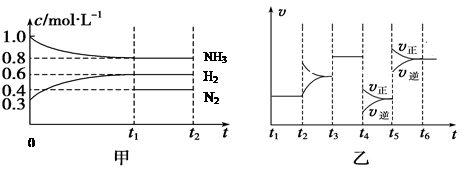
����t1="15" s����t0��t1�εķ�Ӧ����Ϊv(H2)=������
��N2����ʼ���ʵ���Ϊ����������
�۷�Ӧ�ﵽƽ��״̬������˵�����ܱ����Ѵﵽƽ��״̬����
A����λʱ��������a molN2��ͬʱ����3a mol H2 B����������ѹǿ���ٱ仯
C�����������ܶȲ��ٱ仯 D������H��H �����ѵ�ͬʱ������H��N������
��t4ʱ�̸ı������Ϊ���� ��������t5ʱ�̸ı������Ϊ�������� ��
����֪t0��t1�θ÷�Ӧ�ų������յ�����ΪQ kJ(QΪ��ֵ)����д���÷�Ӧ���Ȼ�ѧ����ʽ��____________________________________________________________________
(14��)ij��ѧ��Ӧ2A(g) B(g)+D(g)�����ֲ�ͬ�����½��У�B��D��ʼŨ��Ϊ�㣬��Ӧ��A��Ũ��(mol/L)�淴Ӧʱ��(min)�ı仯����������������ݣ����������գ�
B(g)+D(g)�����ֲ�ͬ�����½��У�B��D��ʼŨ��Ϊ�㣬��Ӧ��A��Ũ��(mol/L)�淴Ӧʱ��(min)�ı仯����������������ݣ����������գ�
| ʵ�� ��� | �¶�/�� | ʱ��/min | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800�� | c 3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820�� | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)��ʵ��l�����У�10 min��20 minʱ������B��ʾ�÷�Ӧ��ƽ����ѧ��Ӧ����Ϊ mol/(L��min)��
(2)��ʵ��2�����У�A�ij�ʼŨ��c2= mol/L����Ӧ��20min�ʹﵽƽ�⣬���Ʋ�ʵ��2�л������������� ��
(3)��ʵ��3�Ļ�ѧ��Ӧ����Ϊv3��ʵ��1�Ļ�ѧ��Ӧ����Ϊv1����v3 v1����c3 1.0 mol/L (���������������=��)��
(4)�Ƚ�ʵ��4��ʵ��l�����Ʋ�÷�Ӧ�� ��Ӧ(����ȡ����ȡ�)��������
��
�����°������·������ʵ�顣
| ʵ���� | ��Ӧ�� | ���� |
| �� | 10mL2% H2O2��Һ | �� |
| �� | 10mL5% H2O2��Һ | �� |
| �� | 10mL5% H2O2��Һ | 1mL0.1mol��L��1FeCl3��Һ |
| �� | 10mL5% H2O2��Һ������HCl��Һ | 1mL0.1mol��L��1FeCl3��Һ |
| �� | 10mL5% H2O2��Һ������NaOH��Һ | 1mL0.1mol��L��1FeCl3��Һ |
��1�������ܼӿ컯ѧ��Ӧ���ʵ�ԭ����_____________________________________��
��2��ʵ��ٺ͢ڵ�Ŀ����____________________________��ʵ��ʱ���ڽϳ�ʱ��û�й۲쵽������������ó����ۡ�������ʾ��ͨ��������H2O2�ȶ������ֽ⡣Ϊ�˴ﵽʵ��Ŀ�ģ����ԭʵ�鷽���ĸĽ���____________________��
��3��д��ʵ��۵Ļ�ѧ��Ӧ����ʽ ��
��4��ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ����ͼ��

������ͼ�ܹ��ó���ʵ�������______________________________________��
��1��25 ��ʱ���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g�� 2NH3��g�� ��H=��92.4 kJ/mol
2NH3��g�� ��H=��92.4 kJ/mol
���ڸ��¶�ʱ��ȡl mol N2��3 mol H2�����ܱ������У��ڴ��������½��з�Ӧ����÷�Ӧ�ų�����������_______92.4 kJ��(�С�ڡ��� �����ڡ� ���ڡ�)
��һ�������£��������淴Ӧ������̶����ܱ������н��У�����������˵����Ӧ�Ѵﵽƽ�����_______________��
| A��NH3���ɵ�������NH3�ֽ��������� |
B���������ķ�Ӧ����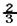 v����NH3��=v����H2�� v����NH3��=v����H2�� |
| C�������ڵ��ܶȲ��ٱ仯 |
| D����λʱ��������a mol N2��ͬʱ����2a mol NH3 |
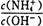 ֵ��_____(����� ����С�� ���䡱)��
ֵ��_____(����� ����С�� ���䡱)����3�������£���0.001mol/LAlCl3��Һ��ͨ��NH3ֱ����������PH=_________ʱ����ʼ���ɳ���(��֪��Ksp[Al(OH)3]=1.0��10-33)
 cC��g������H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
cC��g������H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ�� 

 ���ݴ˻ش��������⣺
���ݴ˻ش��������⣺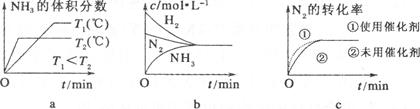
 pC�ﵽƽ�⣬����
pC�ﵽƽ�⣬����