题目内容
【题目】图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线正确的是( )

A. A曲线表示向AlCl3溶液中滴入NaOH溶液至过量
B. B曲线表示向NaAlO2溶液中通入CO2至过量
C. C曲线表示向n(HCl):n(AlC13)=1:1的混合溶液中滴入NaOH溶液至过量
D. D曲线表示向n[Ca(OH)2]:n(KOH)=1:2的混合溶液中通入CO2至沉淀消失
【答案】D
【解析】A.向AlCl3溶液中滴入NaOH溶液至过量,依次发生反应Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O 判断,消耗氢氧化钠是3:1,A项错误;B.向NaAlO2溶液中通入CO2至过量,NaAlO2和CO2反应产生白色沉淀氢氧化铝,沉淀不会溶解于二氧化碳中,B项错误;C.向n(HCl):n(AlC13)=1:1的混合溶液中滴入NaOH溶液至过量,依次发生反应OH-+H+=H2O、Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O;消耗氢氧化钠的量之比是1:3:1,C项错误;D.向n[Ca(OH)2]:n(KOH)=1:2的混合溶液中通入CO2依次发生反应CO2 + Ca2+ +2OH- =CaCO3 ↓+H2O,OH-+CO2═HCO3-,CaCO3+CO2+H2O═Ca(HCO3)2设Ca(OH)2的物质的量为1mol,则KOH的物质的量为2mol,则各段反应消耗的二氧化碳的物质的量分别为1、2、1,D项正确;答案选D.

【题目】通常用碳在高温下还原二氧化硅制得粗硅,粗硅(合铁、铝、硼、磷等杂质)与氯气反应生成四氯化硅(反应温度450-500℃),四氧化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。(D的硬质玻璃管中盛装粗硅)
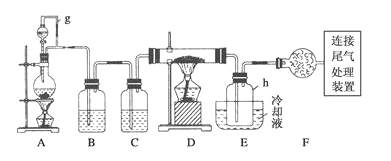
相关信息如下:a.四氧化硅遇水极易反应生成硅酸和氯化氢;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
沸点/℃ | 57.7 | 12.8 | — | 315 | — |
熔点/℃ | -70.0 | -107.2 | — | — | — |
升华温度/℃ | — | — | 180 | 300 | 162 |
请回答下列问题:
(1)写出用碳在高温下还原二氧化硅制得粗硅的化学方程式_________________________。
(2)写出装置A中发生反应的离子方程式__________________________________。
(3)装置A中g管的作用是_________________;装置C中的试剂是____________;
(4)装置E中h瓶收集到的粗产物可通过多次蒸馏得到高纯度四氯化硅,蒸馏后的残留物中,除铁元素外可能还含有的杂质元素是________(填写元素符号)。
(5)写出尾气处理装置中发生反应的离子方程式___________________________。
(6)本题实验装置中有一明显的不足之处,请简述你的改进方案及理由: ___________。