题目内容
为提纯下列物质(括号内的物质为杂质),所选用的除杂试剂和分离方法都正确的是( )
| 被提纯物质 | 除杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| B | CO2(SO2) | 饱和Na2CO3溶液 | 洗气 |
| C | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| D | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用,烷烃及其命名,乙烯的化学性质,乙酸的化学性质,物质的分离、提纯和除杂
专题:有机物的化学性质及推断
分析:A.二者均与NaOH溶液反应;
B.二者均与碳酸钠溶液反应;
C.乙烯被高锰酸钾氧化生成二氧化碳;
D.溴与NaOH溶液反应后与溴苯分层.
B.二者均与碳酸钠溶液反应;
C.乙烯被高锰酸钾氧化生成二氧化碳;
D.溴与NaOH溶液反应后与溴苯分层.
解答:
解:A.二者均与NaOH溶液反应,不能除杂,应选碳酸钠溶液,利用分液法除杂,故A错误;
B.二者均与碳酸钠溶液反应,应选碳酸氢钠溶液,利用洗气法除杂,故B错误;
C.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水,利用洗气法除杂,故C错误;
D.溴与NaOH溶液反应后与溴苯分层,然后分液可除杂,故D正确;
故选D.
B.二者均与碳酸钠溶液反应,应选碳酸氢钠溶液,利用洗气法除杂,故B错误;
C.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水,利用洗气法除杂,故C错误;
D.溴与NaOH溶液反应后与溴苯分层,然后分液可除杂,故D正确;
故选D.
点评:本题考查混合物分离提纯的方法及选择,为高频考点,把握物质的性质及性质差异为解答的关键,侧重除杂的考查,注意除杂的原则即可解答,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
下列有关叙述正确的是( )
| A、测定中和热时,大小两烧杯间填满碎纸的作用是固定小烧杯 |
| B、若用0.010mo1?L-1的氢氧化钠标准溶液滴定未知浓度的盐酸时,滴定前滴定管尖嘴处有气泡,滴定后气泡消失,则测定结果偏小 |
| C、在中和滴定实验中,滴定管用蒸馏水洗涤后,再用标准液润洗,再加进标准液 |
| D、进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化 |
可以证明乙醇分子中有一个氢原子与另外的氢原子不同的是( )
| A、1mol乙醇燃烧生成3mol水 |
| B、1mol乙醇可以生成1mol乙醛 |
| C、1mol乙醇跟足量的金属作用得0.5mol H2 |
| D、乙醇可以制酒精饮料 |
阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
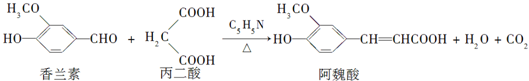
下列说法正确的是( )

下列说法正确的是( )
| A、可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 |
| B、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种 |
| C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D、香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应 |
下列反应属于氮的固定的是( )
| A、Cl2将NH3氧化成N2 |
| B、NH3和HCl生成NH4Cl固体 |
| C、豆科植物将N2转化为NH4+ |
| D、空气中的氮氧化物转化成酸雨 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+.某同学为了确认其成分,取部分试液,设计并完成了如下实验:
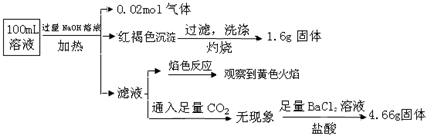
由此可知原溶液中( )

由此可知原溶液中( )
| A、原溶液中c(Fe3+)=0.2mol?L-1 |
| B、溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2mol?L-1 |
| C、SO42-、NH4+、Na+一定存在,CO32-、Al3+一定不存在 |
| D、要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+ |