题目内容
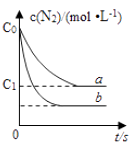
【题目】在t℃时,某NaOH稀溶液中,c(H+)=10﹣a mol/L,c(OH﹣)=10﹣b mol/L,已知a+b=13,则在该温度下,将100mL 0.10mol/L的稀硫酸与100mL 0.40mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)( )
A.11.52
B.11.70
C.11.82
D.12.00
【答案】D
【解析】解:水的离子积常数Kw=c(H+)c(OH﹣)=10﹣a×10﹣b=10﹣(a+b)=10﹣13 ,
而稀H2SO4溶液与NaOH反应的关系式:
H2SO4 | ~ | 2NaOH |
1 | 2 | |
100mL×0.1molL﹣1 | 200mL×0.1molL﹣1 |
碱过量,过量的碱为:0.02mol,则c(OH﹣)= ![]() =0.1molL﹣1 , 所以c(H+)=
=0.1molL﹣1 , 所以c(H+)= ![]() =
= ![]() =10﹣12molL﹣1 , PH=12,故选D.
=10﹣12molL﹣1 , PH=12,故选D.

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】化学课外活动小组利用以下装置完成系列实验.请回答以下问题: 
(1)装置甲中仪器a的名称为 . 用装置甲制取NH3 , 在b中加入CaO固体,a中加入浓氨水,写出反应的化学方程式: .
(2)将C12持续通入装有淀粉一KI无色溶液的装置乙中,溶液变蓝而后逐渐褪色.查阅资料得知:溶液蓝色逐渐褪色,是因为有+5价的碘元素生成.请写出该反应的离子方程式: .
(3)用装置丙模拟“氨的催化氧化”实验.锥形瓶内装有浓氨水,通入空气,并将红热的铂丝插入锥形瓶内,铂丝保持红热.铂丝保持红热的原因是;锥形瓶内还可观察到现象是 .
(4)活动小组从“绿色化学”角度出发.在装置丁中进 行SO2的性质实验.其中棉花上蘸有不同试剂.请填写表中空白:
棉花位置 | ① | ② | ③ |
棉花上蘸有的试剂 | 品红溶液 | 酸性高锰酸钾溶液 | |
现象 | 溶液紫色褪去 | 无 | |
结论 | SO2具有漂白性 | SO2具有 | SO2有毒,不能排空 |