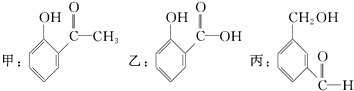
题目内容
【题目】含苯酚的工业废水的处理流程如图所示. 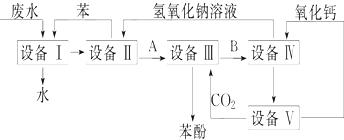
(1)①流程图设备Ⅰ中进行的是操作(填写操作名称).实验室里这一步操作可以用(填仪器名称)进行. ②由设备Ⅱ进入设备Ⅲ的物质A是(填化学式,下同).由设备Ⅲ进入设备Ⅳ的物质B是 .
③在设备Ⅲ中发生反应的化学方程式为 .
④在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和 . 通过(填操作名称)操作,可以使产物相互分离.
⑤图中,能循环使用的物质是:、、C6H6和CaO.
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是 .
(3)为测定废水中苯酚的含量,取此废水100mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331g,则此废水中苯酚的含量为mg/L.
【答案】
(1)萃取、分液;分液漏斗;C6H5ONa;NaHCO3;C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;CaCO3;过滤;CO2;NaOH
(2)向污水中滴加FeCl3溶液,若溶液呈紫色,则表明污水中有苯酚
(3)940
【解析】解:(1)①工业废水与苯进入设备Ⅰ得到苯酚、苯的溶液与可以排放的无酚工业废水,说明在设备Ⅰ中进行的是萃取,利用苯与苯酚相似的结构互溶与水不溶,将苯酚从工业废水里提取出来,用分液的方法将下层的工业废水放出排放,上层的苯酚、苯混合液进入设备Ⅱ;萃取、分液必须用到的仪器名称叫分液漏斗,所以答案是:萃取、分液;分液漏斗;②盛有苯酚、苯溶液的设备Ⅱ中注入氢氧化钠溶液,此时,具有酸性的苯酚跟氢氧化钠发生反应,生成苯酚钠和水,由设备Ⅱ进入设备Ⅲ的物质A是C6H5ONa,在设备Ⅱ中的液体分为两层,上层是苯层,下层是苯酚钠的水溶液,上层的苯通过管道送回设备Ⅰ中继续萃取工业废水中的苯酚,循环使用,下层的苯酚钠溶液进入设备(Ⅲ);在盛有苯酚钠溶液的设备Ⅲ中,通入过量的二氧化碳气,发生化学反应,生成苯酚和碳酸氢钠,所以答案是:C6H5ONa;NaHCO3; ③依据碳酸性比苯酚的酸性强,弱酸盐与“强”酸发生的复分解反应,二氧化碳和苯酚钠反应生成苯酚,反应的方程式为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 , 所以答案是:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;④盛有碳酸氢钠溶液的设备Ⅳ中,加入生石灰,生石灰与碳酸氢钠溶液里的水反应生成氢氧化钙,熟石灰和与碳酸氢钠发生复分解反应,生成沉淀;溶液与沉淀通过过滤分离,所以答案是:CaCO3;过滤; ⑤设备Ⅴ应是石灰窑,CaCO3高温分解所得的产品是氧化钙和二氧化碳,所得二氧化碳通入设备Ⅲ,反应所得氧化钙进入设备Ⅳ.在含苯酚工业废水提取苯酚的工艺流程中,苯、氧化钙、CO2、和NaOH理论上应当没有消耗,它们均可以循环使用,所以答案是:CO2、NaOH;(2)苯酚和氯化铁溶液之间会发生显色反应,向溶液中滴加FeCl3溶液,若溶液呈紫色,则表明污水中有苯酚,所以答案是:向污水中滴加FeCl3溶液,若溶液呈紫色,则表明污水中有苯酚;(3)发生反应为苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于取代,反应的化学方程式为: 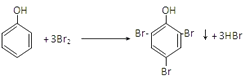 ,得到沉淀0.331g为三溴苯酚,其物质的量为:
,得到沉淀0.331g为三溴苯酚,其物质的量为: ![]() =0.001mol,则100mL 该废水中含有苯酚的物质的量为0.001mol,质量为:94g/mol×0.001mol=0.094g,此废水中苯酚的含量为:
=0.001mol,则100mL 该废水中含有苯酚的物质的量为0.001mol,质量为:94g/mol×0.001mol=0.094g,此废水中苯酚的含量为: ![]() =0.94g/L=940mg/L,
=0.94g/L=940mg/L,
所以答案是:940.