题目内容
17.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM25(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM25、SO2、NOx等进行研究具有重要意义.请回答下列问题:(1)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.
已知:H2(g)+$\frac{1}{2}{O_2}(g)={H_2}$O(g)△H=-241.8kJ•mol-1
C(s)+$\frac{1}{2}{O_2}$(g)=CO(g)△H=-110.5kJ•mol-1
写出焦炭与水蒸气反应的热化学方程式:C(s)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol.
②洗涤含SO2的烟气.以下物质可作洗涤剂的是ab.
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(2)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0若1mol空气含0.8molN2和0.2molO2,1300°C时在密闭容器内反应达到平衡,测得NO为8×10-4mol.计算该温度下的平衡常数K≈4×10-6.
汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是该反应是吸热反应,温度升高,反应速率加快,平衡向正方向移动,单位时间内产生的NO多.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为该反应的△H>0,△S<0,所以△H-T△S>0.
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为2XCO+2N0X 2XCO2+N2.
分析 (1)①利用盖斯定律,通过已知热化学方程式运算得目标热化学方程式;
②依据二氧化硫的性质:是一种酸性氧化物可以和碱反应,二氧化硫溶于水得亚硫酸,酸性强于碳酸,所以可以和碳酸钠溶液反应;
(2)①列三段表示出各种物质平衡时的浓度,带入平衡常数表达式;N2(g)+O2(g)?2NO(g)△H>0,该反应是吸热反应,温度升高,反应速率加快,平衡向正方向移动,单位时间内产生的NO多;
②利用反应能否自发进行的判据△H-T△S;
③CO和NOx在催化剂的作用下发生氧化还原反应生成无毒的二氧化碳和氮气.
解答 (2)①H2(g)+$\frac{1}{2}$O2(g)=H20 (g)△H=-241.8kJ•mol-1 ①
C(s)+$\frac{1}{2}$O2(g)=CO (g)△H=-110.5kJ•mol-1②
利用盖斯定律将方程式变形:②-①得 C(s)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol,
故答案为:C(s)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol;
②二氧化硫是酸性氧化物所以具有酸性氧化物的通性能够与碱反应:SO2+Ca(OH)2=CaSO3↓+H2O;
二氧化硫水溶液是亚硫酸所以也能够与碳酸钠反应:SO2+Na2CO3=Na2SO3+CO2↑所以可以用氢氧化钙溶液和碳酸钠溶液做洗涤剂;
二氧化硫与氯化钙溶液不反应,且在亚硫酸氢钠溶液中的溶解度很小,所以不能用氯化钙和亚硫酸氢钠溶液做洗涤液,
故答案为:ab;
(3)①设反应容器的体积是aL
根据题意得:
N2(g)+O2(g)?2NO(g)
初始浓度 $\frac{0.8}{a}$ $\frac{0.2}{a}$ 0
转化浓度 $\frac{4×1{0}^{-4}}{a}$ $\frac{4×1{0}^{-4}}{a}$ $\frac{8×1{0}^{-4}}{a}$,
平衡浓度 $\frac{0.8}{a}$-$\frac{4×1{0}^{-4}}{a}$$\frac{0.2}{a}$-$\frac{4×1{0}^{-4}}{a}$$\frac{8×1{0}^{-4}}{a}$
将各种物质的浓度带入表达式 得K=$\frac{{c}^{2}(NO)}{c({N}_{2})c({O}_{2})}$≈4×10-6,
故答案为:4×10-6;
汽缸中发生的化学反应:N2(g)+O2(g)?2NO(g)△H>0,这是个吸热反应,温度升高,反应速率加快,平衡向正方向移动,单位时间内产生的NO多,
故答案为:该反应是吸热反应,温度升高,反应速率加快,平衡向正方向移动,单位时间内产生的NO多;
②2CO(g)=2C(s)+O2(g)是一个熵值减小的反应即:△S<0,同时又是一个△H>O,所以△H-T△S一定大于0,所以任何条件下不能自发进行,
故答案为:不能实现,因为该反应的△H>0,△S<0,所以△H-T△S>0;
③CO和NOx在催化剂发生反应:2XCO+2N0X 2XCO2+N2,故答案为:2XCO+2N0X 2XCO2+N2.
点评 本题考查了pH值的计算、盖斯定律求反应热、化学平衡常数的计算、反应进行方向的判断,题目综合性非常强,涉及知识点多,难度中等,同时又结合了环境的污染和治理,题目又比较新颖,是高考的热门话题,解题时应该结合相应的知识,认真解答.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案(1)小明通过一玻璃管向盛有澄清石灰水的试管中吹气,溶液变浑浊
(2)小丽向盛有澄清石灰水的试管中加入适量的碳酸钠溶液,溶液变浑浊.
(3)小倩向盛有少量氢氧化钙固体的试管中加入一定量的蒸馏水,液体变浑浊,再向其中加入3滴无色酚酞,液体变成红色,继续向试管中加入过量的稀盐酸,出现的现象是红色褪去,浑浊液体变澄清,据小倩同学的实验及现象可知氢氧化钙具有的性质有微溶于水、能使酚酞变红、能与(盐)酸反应.
(4)上述实验涉及的反应不属于碱的相似化学性质的反应方程式是Ca(OH)2+Na2CO3=CaCO3↓+2 NaOH,不属于基本反应类型的反应方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
(5)实验后三位同学将试管中的废液倒入同一烧杯中,搅拌,得到无色溶液,则该溶液中一定含有的物质是NaCl、CaCl2、(酚酞)(或氯化钠、氯化钙(酚酞)).请设计实验证明可能存在的物质是否存在:
| 实验步骤 | 实验现象及结论 |
| 取实验所得的无色溶液少量于试管中,向试管中滴加石蕊溶液(或锌粒、碳酸钠等) | 溶液由无色变成红色(或有气泡冒出)说明溶液中还含有HCl |
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③⑤⑥ | D. | ①③④⑥ |
| A. | 二氧化硅用于制作电脑芯片和光导纤维 | |
| B. | 硫磺用于配制黑火药和工业生产硫酸 | |
| C. | 氯气用于城市自来水消毒和生产漂白粉 | |
| D. | 钾钠合金用作原子反应堆的导热剂 |
| A. |  | B. |  | C. |  | D. |  |
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 21.2 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
某同学设计用物质的量之比为1:1的硝酸钠和氯化钾为原料,加入一定量的水制取硝酸钾的实验,其流程如图所示:
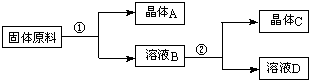
(1)在①和②的实验过程中,需要控制的关键的实验条件是控制温度,在上述晶体中,C(填“A”或“C”)应为硝酸钾晶体.
(2)在①的实验过程中,需要进行的操作依次是加水溶解、蒸发浓缩、趁热过滤.
(3)粗产品中可能含有杂质离子Na+、Cl-,检验其中一种离子的方法是用洁净的铂丝或铁丝蘸取粗产品在火焰上灼烧,若火焰呈黄色,证明有Na+;或 取粗产品少许,加水配成溶液,加入硝酸酸化的硝酸银溶液,若有白色沉淀产生,证明有Cl-.
(4)为了洗涤所得的硝酸钾晶体,下列溶剂可用作洗涤剂的是bc(填编号).
a.热水 b.冰水 c.95%的酒精 d.四氯化碳
(5)如取34.0g硝酸钠和29.8g氯化钾,加入70g水,在100℃蒸发掉50g水,维持该温度,过滤,析出晶体的质量为15.58g.
| A. | v(O2)=0.125mol•(L•s)-1 | B. | v(NO)=0.01mol•(L•s)-1 | ||
| C. | v(NH3)=0.01 mol•(L•s)-1 | D. | v(NH3)=0.2 mol•(L•s)-1 |
| A. | 氯原子的结构示意图: | |
| B. | 作为相对原子质量测定标准的碳核素:614C | |
| C. | CCl4的电子式 | |
| D. | 氯化镁的电子式: |
