题目内容
Ⅰ.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。下表为一些化学键的键能数据
| 化学键 | Si-Si | O=O | Si-O |
| 键能/kJ·mol-1 | a | b | c |
写出硅高温燃烧的热化学方程式 。
Ⅱ.利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如右图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。写出下列电解池中总反应的离子方程式:
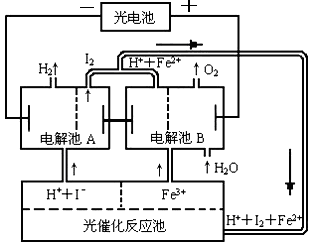
电解池A 。
电解池B 。
(2)若电解池A中生成3.36 L H2(标准状况),计算电解池B中生成Fe2+的物质的量为 mol。
Ⅲ.在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)
 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。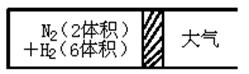
请据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2 和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同。
①a=1,c=2,则b= 。在此情况下,反应起始时将向 反应方向(填“正”或“逆”)进行。
②若需规定起始时反应向逆方向进行,则c的取值范围是 。
(2)在上述恒压装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是 ,原因是 。
Ⅰ.Si(s)+O2(g) SiO2(s) △H=(2a+ b - 4c)kJ/mol(2分)
SiO2(s) △H=(2a+ b - 4c)kJ/mol(2分)
Ⅱ.(1)A 池 2H+ +2I-=H2↑ + I2(2分) B 池 4Fe3+ + 2H2O=4Fe2+ + O2↑+ 4H+(2分)
(2)0.300mol(2分)
Ⅲ.(1)① 3 (2分)逆(1分)② 1<c≤4 (2分)
(2)降低温度 (1分) 降低温度平衡向正反应方向移动,气体总分子数减少(2分)
解析试题分析:Ⅰ.硅是原子晶体,平均1个硅原子形成2个Si-Si键。二氧化硅是原子晶体,平均1个硅原子形成4个Si-O键。又因为反应热等于断键吸收的能量与形成化学键所放出的能量的差值,因此硅高温燃烧的热化学方程式为Si(s)+O2(g) SiO2(s) △H=(2a+ b - 4c)kJ/mol。
SiO2(s) △H=(2a+ b - 4c)kJ/mol。
Ⅱ.(1)电解池左边放出氢气,氢离子在此得到电子,发生还原反应,则碘离子失去电子发生氧化反应,故A池中总反应式为2H+ +2I-=H2↑ + I2;电池右侧放出氧气,说明溶液中的氢氧根失去电子发生氧化反应,则溶液中的铁离子得到电子发生还原反应,因此B池总反应式为4Fe3+ + 2H2O=4Fe2+ + O2↑+ 4H+。(2)若电解池A中生成3.36 L H2(标准状况),其中氢气的物质的量是3.36L÷22.4L/mol=0.15mol,转移电子0.3mol,所以根据得失电子守恒可知B池中生成亚铁离子的物质的量是0.3mol。
Ⅲ.(1)①反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同,恒温恒压条件下,采用极限分析法,c体积的氨气完全转化为氮气和氧气之比是1:3,所以只要a:b=2:6,则b=3a=3,因反应前混合气体为8体积,反应后混合气体为7体积,体积差为1体积,由差量法可解出平衡时氨气为1体积;而在起始时,氨气的体积为c=2体积,比平衡状态时大,为达到同一平衡状态,氨的体积必须减小,所以平衡逆向移动;
②若需让反应逆向进行,由上述①所求出的平衡时氨气的体积为1可知,氨气的体积必须大于1,最大值则为2体积氮气和6体积氢气完全反应时产生的氨气的体积,即为4体积,则1<c≤4;
(2)根据6.5<7可知,上述平衡应向体积缩小的方向移动,即向放热方向移动,所以采取降温措施,这是由于降低温度平衡向正反应方向移动,气体总分子数减少。
考点:考查热化学方程式的书写、电化学原理的应用、以及可逆反应的有关计算与判断

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案(14分)图a是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图。根据题意回答下列问题
(1)写出NO2和CO反应的热化学方程式 。
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)= 。
(3)此温度下该反应的平衡常数K= ;温度降低,K (填“变大”、“变小”或“不变”)
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol NO2 1 mol CO | 2 mol NO 2 mol CO2 | 1 mol NO2、1 mol CO 1 mol NO、1 mol CO2 |
| 平衡时c(NO) /mol·L-1 | 1.5 | 3 | m |
| 能量变化 | 放出a kJ | 吸收b kJ | 放出c kJ |
| CO或NO的转化率 | α1 | α2 | α3 |
则:α1+α2= , a+b/2= ,m=
(17分)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物。工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。
(1) 已知:CH4、H2和CO的燃烧热分别为890.3kJ/mol、285.8kJ/mol和283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ。写出甲烷与水蒸气在高温下反应制取合成气的热化学方程式 。
(2)在一定条件下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
  时间/min 时间/min物质 浓度 | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol·L—1 | 0.13 mol·L—1 | 0.1 mol·L—1 | 0.1 mol·L—1 | 0.09 mol·L—1 |
| H2 | 0 mol·L—1 | 0.2 mol·L—1 | 0.3 mol·L—1 | 0.3 mol·L—1 | 0.33 mol·L—1 |
②3min时改变的反应条件是____________________(只填一种条件的改变)
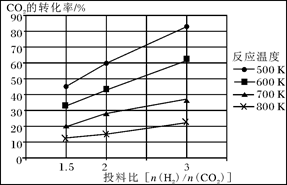
(3)已知温度、压强、投料比X〔n(CH4)/n(H2O)〕对该反应的影响如图所示。

①图1中的两条曲线所示投料比的关系X1____X2(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:p1_______p2
(4)以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池
①放电时,正极的电极反应式_______________________________________
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 ____。
(16分)工业合成氨与制备硝酸一般可连续生产,流程如下: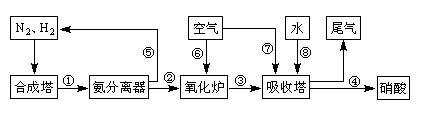
(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g) CO2(g)+H2(g)。t℃时,往10L密闭容器中充入2mol CO和3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。则该温度下此反应的平衡常数K= (填计算结果)。
CO2(g)+H2(g)。t℃时,往10L密闭容器中充入2mol CO和3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。则该温度下此反应的平衡常数K= (填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g) △H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1 300℃(填“>”、“<”或“=”)。
2NH3(g) △H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1 300℃(填“>”、“<”或“=”)。
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
(3)氨气在纯氧中燃烧生成一种单质和水,科学家利用此原理,设计成“氨气-氧气”燃料电池,则通入氨气的电极是 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为 。
(4)用氨气氧化可以生产硝酸,但尾气中的NOx会污染空气。目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H= -1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为 。
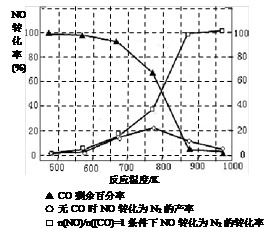
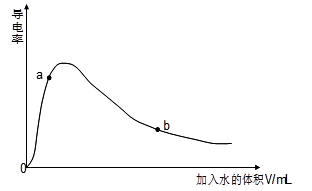
(5)某研究小组在实验室以“Ag-ZSM-5”为催化剂,测得将NO转化为N2的转化率随温度变化情况如图。据图分析,若不使用CO,温度超过775K,发现NO的转化率降低,其可能的原因为 ;在n(NO)/n(CO)=1的条件下,应控制的最佳温度在 左右。
 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)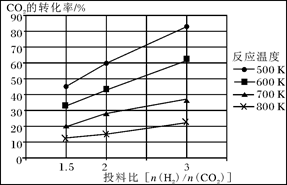
 H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol
H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol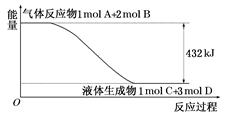
 C6 H5- CH=CH2 (g) +H2(g) ΔH1
C6 H5- CH=CH2 (g) +H2(g) ΔH1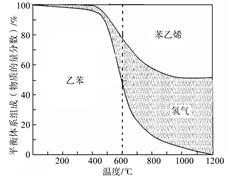
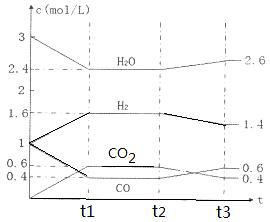
 CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。
CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。