题目内容
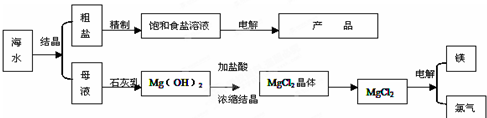
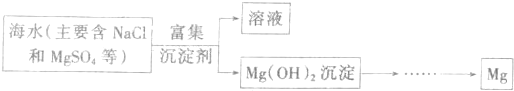
从海水中提取镁的主要流程是( )
A.海水
| |||||||
B.海水
| |||||||
C.海水
| |||||||
D.海水
|
海水提取金属镁的流程:第一步应该是将海水的中镁离子富集起来,常用的方法是沉淀,应该是②MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;第二步应该是④过滤得到氢氧化镁沉淀;第三步应该是制备氯化镁溶液,Mg(OH)2+2HCl═MgCl2+2H2O;第四步应该是氯化镁溶液浓缩结晶制备熔融的氯化镁;最后一步应该是⑤电解熔融的氯化镁MgCl2
Mg+Cl2↑;
故选:A.
| ||
故选:A.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目