题目内容
【题目】某高分子化合物R的结构简式如图,下列有关R的说法正确的是
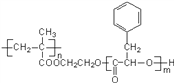
A. R的单体之一的分子式为C9H10O2
B. R完全水解后生成物均为小分子有机物
C. 碱性条件下,1molR完全水解消耗NaOH的物质的量为2mol
D. 通过加聚反应和缩聚反应可以生成R
【答案】D
【解析】A. 由结构可知,R的单体为CH2=C(CH3)COOH、OHCH2CH2OH、HOOCCHOHCH2C6H5,R的单体之一的分子式为C9H10O3,故A错误;B. R完全水解生成乙二醇和两种高分子化合物,故B错误;C. 1molR中含n(1+m)molCOOC,则碱性条件下,1molR完全水解消耗NaOH的物质的量为n(m+1)mol,故C错误;D.单体中存在C=C、OH、COOH,则通过加聚反应和缩聚反应可以生成R,故D正确;答案选D。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:________________。
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式:_______________。
(3)“调pH”时pH的调控范围为_____________,试用化学反应原理的相关知识解释滤渣Ⅱ的生成:______________________________________________________。
(4)写出“沉镍”时发生反应的离子方程式:__________________________________,证明Ni2+已经沉淀完全的实验步骤及现象是___________________________________,当Ca2+沉淀完全时,溶液中c(F-)>____________mol·L-1(写出计算式即可)。
(5)操作a的内容是_________________________________________________________。
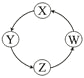
【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①②③ B. ①③④ C. ②③ D. ①④