题目内容
下列关于氯的说法正确的是
| A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂 |
| B.若1735Cl、1737Cl为不同的核素,有不同的化学性质 |
| C.实验室制备Cl2,可用排饱和食盐水法收集 |
| D.1.12 LCl2含有1.7NA个质子(NA表示阿伏伽德罗常数) |
C
解析试题分析:A选项。氯气的化合价为0,处于中间价态,既可以升高也可以降低。所以它既可以做氧化剂又可以做还原剂。所以A选项是错误的。B选项化学性质由最外层电子数决定,而两种核素1735Cl、1737Cl的核外电子数都为17,它们的最外层电子数都为7,因此它们具有相同的化学性质。所以B选项是错误的。C选项,制备氯气时,常常会有杂质氯化氢,而氯化氢易溶于饱和食盐水,而氯气在饱和食盐水中的溶解度非常的小,所以C选项是正确的。D选项没有指明温度和压强,所以不能计算。D选项是错误的。
考点:元素及化合物的性质

练习册系列答案
相关题目
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( ) 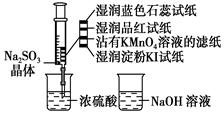
| A.蓝色石蕊试纸先变红后褪色 |
| B.品红试纸、沾有KMnO4溶液滤纸均褪色都能证明SO2的漂白性 |
| C.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2 |
| D.NaOH溶液和品红溶液均可用于除去实验中多余的SO2 |
向硝酸钠溶液中加入铜粉不发生反应,若再加入(或通入)某种物质,则铜粉可以逐渐溶解,不符合此条件的物质是
| A.Fe(NO3)3 | B.HCl | C.NaHSO4 | D.NaHCO3 |
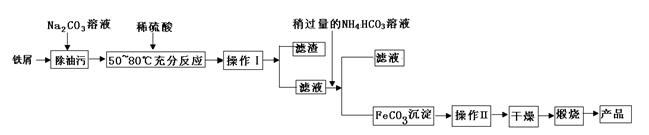
工业上用洗净的废铜屑作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法是
| A.Cu+HNO3(浓)→ Cu(NO3)2 | B.Cu+HNO3(稀)→ Cu(NO3)2 |
C.Cu 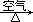 CuO CuO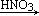 Cu(NO3)2 Cu(NO3)2 | D.Cu 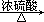 CuSO4 CuSO4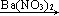 Cu(NO3)2 Cu(NO3)2 |
已知氨气可与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是 ( )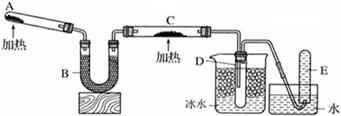
| A.反应中氧化剂和还原剂的物质的量之比为2∶3 |
| B.装置B中加入的物质可以是碱石灰或无水氯化钙 |
| C.装置D中液体可以使干燥的红色石蕊试纸变蓝 |
| D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气 |
下列溶液中能够区别SO2和CO2气体的是
①澄清石灰水 ②KMnO4酸性溶液 ③氯水 ④品红溶液
| A.①③④ | B.②③④ | C.①②③ | D.全部 |
下列关于浓硫酸的说法中,不正确的是
| A.常作为气体的干燥剂 | B.滴在蔗糖上,蔗糖会变黑 |
| C.常温下不能与铁发生反应 | D.工业上主要采用接触法制备 |
2014年世界环境日中国主题为“向污染宣战”,下列有关环境污染的叙述错误的是( )
| A.大气污染主要指CO、SO2、氮氧化物以及粉尘等 |
| B.氮氧化物是造成光化学烟雾的主要原因 |
| C.臭氧可以杀菌消毒,空气中的臭氧含量越高,对人体健康越有利 |
| D.酸雨通常是指pH在5.6以下的降水 |