题目内容
某元素最高价氧化物的化学式是R2O5,已知R气态氢化物中含氢8.82%.试计算R的相对原子质量,写出R最高价氧化物水化物的化学式并判断其酸性的强弱.
答案:
解析:
提示:
解析:
|
【解答】设R的相对原子质量为x,则有 所以R的相对原子质量为31,为磷元素,其最高价氧化物水化物的化学式为H3PO4. H3PO4酸性比较: 同一横行比较:H2SiO3<H3PO4<H2SO4, 同一纵行比较:H3AsO4<H3PO4<HNO3. 【巧解导析】由化学式R2O5知R的最高正价为+5,其负价为-3,氢化物化学式为RH3,由H的含量可求R的相对原子质量: H%= |
提示:
|
【巧解点悟】解本题的关键是正确书写气态氢化物的化学式,否则难以得出正确结果. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
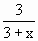 ×100%=8.82%,解得x=31.
×100%=8.82%,解得x=31.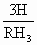 ×100%.
×100%.
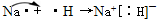


 ,质量数A是137,中子数N
,质量数A是137,中子数N