题目内容
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)  Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O  HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO  H+ + ClO- Ka=?
H+ + ClO- Ka=?
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是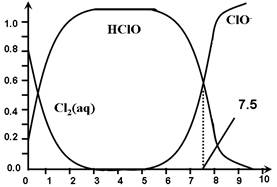
A.Cl2(g)+ H2O  2H+ + ClO- + Cl- K=10-10.9 2H+ + ClO- + Cl- K=10-10.9 |
| B.在氯处理水体系中,c(HClO) + c(ClO-) =c(H+)-c(OH-) |
| C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差 |
| D.氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
C。
解析试题分析:A.Cl2(g)+ H2O  2H+ + ClO-+ Cl-,可将前两个方程式相加,K=K1·K2=10-4.6,A错;B.在氯处理水体系中,电荷守恒c(OH-)+c(ClO-) =c(H+),故B错;C.图中HClO在pH=7.5时的比pH=6.5时少,杀菌效果差,正确;夏季温度高,HClO易分解,故杀菌效果比在冬季差。
2H+ + ClO-+ Cl-,可将前两个方程式相加,K=K1·K2=10-4.6,A错;B.在氯处理水体系中,电荷守恒c(OH-)+c(ClO-) =c(H+),故B错;C.图中HClO在pH=7.5时的比pH=6.5时少,杀菌效果差,正确;夏季温度高,HClO易分解,故杀菌效果比在冬季差。
考点:溶液中的微粒图像解析。

练习册系列答案
相关题目
常温时,下列叙述正确的是
| A.pH=9的NH4Cl与NH3?H2O混合溶液中c(Cl-)>c(NH4+) |
| B.pH=2.5的可乐中c(H+) 是pH=3.5的柠檬水中c(H+)的10倍 |
| C.AgCl在0.1mol /L CaCl2溶液和0.1mol/L NaCl溶液中的溶解度相同 |
| D.1 mL 1mol /L Na2CO3溶液加水稀释至100mL, pH和Kw均减小 |
下列物质的制取,实验操作正确的是
| A.将CuCl2溶液置于蒸发皿中加热蒸干,可制取无水CuCl2固体 |
| B.将NH4HCO3饱和溶液置于蒸发皿中加热蒸于,可制取NH4HCO3固体 |
| C.向FeCl3饱和溶液中缓慢滴入过量氨水加热,可制取Fe(OH)3胶体 |
| D.向电石中缓慢滴入饱和食盐水,可制取C2H2 |
室温下,对pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,其中叙述正确的是
| A.温度升高20℃后,两溶液pH均不变 |
| B.加适量的醋酸钠晶体后,两溶液的pH均增大 |
| C.加水稀释2倍后,两溶液的pH同等程度减小 |
| D.加足量的锌充分反应后,两溶液中产生的氢气一样多 |
下列有关电解质溶液中粒子浓度关系正确的是
| A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) |
| B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-) |
| C.CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-) |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)] |
室温下,下列溶液中粒子浓度大小关系正确的是
| A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) |
| B.Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) |
| C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) |
| D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
| A.c(Ca2+)、c(OH-)均增大 | B.c(Ca2+)、c(OH-)均保持不变 |
| C.c(Ca2+)、c(OH-)均减小 | D.c(OH-)增大、c(H+)减小 |
下列各项说法中,不正确的是 ( )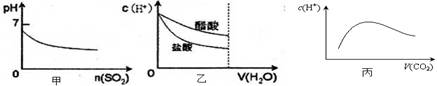
| A.甲是向溴水通入SO2气体时,pH与SO2物质的量的关系图 |
| B.乙是向c(H+)相同的醋酸和盐酸滴入水时,c(H+)与水体积的关系图 |
| C.常温常压下,将2b mol CO2气体通入1L bmol·L-1的NaOH溶液中,随着CO2气体的通入,溶液中由水电离出的c(H+)有如丙图变化关系 |
| D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)>c(NO3-) |
某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中正确的是
| A.pH=1和pH=2的盐酸,c(H+)之比为1:2 |
| B.物质A三态间的转化如下:A(g)→A(1)→A(s),则该转化过程中△S<O |
| C.pH=13的强碱溶液,加水稀释后,溶液中所有离子的浓度均变小 |
| D.pH=9的CH3COONa溶液和pH=9的NH3.H2O溶液,两溶液中水的电离程度相同 |