题目内容
17.常温下,下列各组离子一定能大量共存的是( )| A. | [H+]=10-12mol•L-1的溶液:K+、Ba2+、Cl-、Br- | |
| B. | 滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- | |
| C. | $\frac{O{H}^{-}}{{H}^{+}}$=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | 由水电离的[H+]=1.0×10-13 mol•L-1的溶液中:K+、NH4+、[Al(OH)4]-、HCO3- |
分析 A.[H+]=10-12mol•L-1的溶液,显碱性;
B.滴加甲基橙试剂显红色的溶液,显酸性,离子之间发生氧化还原反应;
B.$\frac{O{H}^{-}}{{H}^{+}}$=1012的溶液,显碱性;
D.由水电离的[H+]=1.0×10-13 mol•L-1的溶液,为酸或碱溶液.
解答 解:A.[H+]=10-12mol•L-1的溶液,显碱性,该组离子之间不反应,可大量共存,故A正确;
B.滴加甲基橙试剂显红色的溶液,显酸性,H+、Fe2+、NO3-发生氧化还原反应,不能大量共存,故B错误;
B.$\frac{O{H}^{-}}{{H}^{+}}$=1012的溶液,显碱性,碱性溶液中不能大量存在NH4+、Al3+,且Al3+、CO32-相互促进水解,不能大量共存,故C错误;
D.由水电离的[H+]=1.0×10-13 mol•L-1的溶液,为酸或碱溶液,酸溶液中不能大量存在[Al(OH)4]-、HCO3-,碱溶液中不能大量存在NH4+、HCO3-,且[Al(OH)4]-促进HCO3-的电离,不能大量共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意离子之间的氧化还原反应、水解反应的判断,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
8.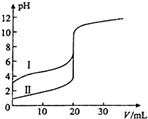 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )| A. | Ⅱ表示的是滴定盐酸的曲线 | |
| B. | PH=7时,滴定盐酸消耗V(NaOH)大于滴定醋酸消耗V(NaOH) | |
| C. | V(NaOH)=20ml时,C(Cl-)═C(CH3COO-) | |
| D. | V(NaOH)=10ml时,醋酸溶液中:C(CH3COO- )>C(Na+ )>C(H+)>C(OH-) |
12.下列过程中,需吸收能量的是( )
| A. | H+H→H2 | B. | 天然气燃烧 | C. | I2→I+I | D. | S+O2→SO2 |
2.同温同压下两个容积相等的贮气瓶,一个装有NO气体,另一个装有N2和O2的混合气体,两瓶内的气体一定具有相同的( )
| A. | 质量 | B. | 原子总数 | C. | 质子总数 | D. | 密度 |
6.在同一容器内有X、Y、Z、Q四种物质,在合适的条件下反应,反应前后各物质的质量如下表,该反应一定属于( )
| X | Y | Z | Q | |
| 反应前g | 20 | 20 | 20 | 205 |
| 反应后g | 10 | 20 | 26 | 24 |
| A. | 氧化还原反应 | B. | 分解反应 | C. | 离子反应 | D. | 复分解反应 |