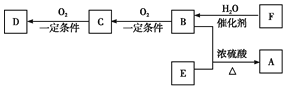
题目内容
【题目】下面是甲、乙、丙三位同学制备乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
(实验目的) 制取乙酸乙酯
(1).(实验原理) 甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸作吸水剂和__________。
(2).(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:
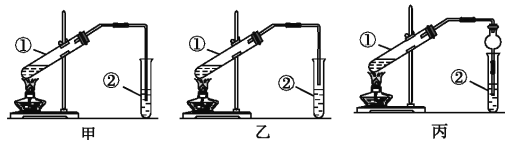
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是______(填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是__________。
(实验步骤)
①按你选择的装置组装仪器,在试管中先加入3mL乙醇,然后边振荡试管①边慢慢加入2mL浓H2SO4和2mL乙酸;
②将试管①固定在铁架上;
③在试管②中加入适量的饱和Na2CO3溶液;
④用酒精灯对试管①缓慢加热;
⑤当观察到试管②中有明显现象时停止实验。
(3).(问题讨论)
a.步骤(1)装好实验装置,加入样品前还应检查__________;
b.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有:无色油状液体、__________;
c.试管②中分离出乙酸乙酯的实验操作是__________。
d.写出制备乙酸乙酯的化学方程式:__________。
【答案】催化剂 乙 防止倒吸 装置的气密性 不溶于水、有香味 分液 CH3COOH+C2H5OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
【解析】
乙醇、乙酸与浓硫酸混合共热制取乙酸乙酯,浓硫酸的作用是做吸水剂和催化剂。因为乙醇和乙酸易挥发,所以该反应生成的乙酸乙酯中含有一定量的乙醇和乙酸。乙醇和乙酸都易溶于水,乙酸可与碳酸钠反应,且加热过程中反应器中的蒸气压不稳定,因此,导气管不能直接插入碳酸钠溶液以防引起倒吸,据此分析作答。
[实验原理]乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水,浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂;
[装置设计]乙酸和乙醇易溶于水,导管插入液面下容易发生倒吸,所以为了防止倒吸,导管不能插入液面以下,应该选乙装置;球形干燥管导气的同时也起到防倒吸作用,故答案为诶:乙;防止倒吸;
[问题讨论] a.步骤(1)装好实验装置,加入样品前还应检查装置的气密性;
b. 乙酸乙酯在混合液上层,说明乙酸乙酯不溶于水、密度比水小,还能够闻到香味,说明乙酸乙酯具有特殊香味,故答案为:不溶于水、有香味;
c. 乙酸乙酯不溶于饱和碳酸钠溶液,混合液会分层,分离乙酸乙酯的方法为分液;
d. 乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;