题目内容
一定温度下,在氢氧化钙的悬浊液中,存在氢氧化钙固体与其电离出的离子间溶解结晶平衡:Ca(OH)2(s) 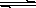 Ca2+(aq)+2OHˉ(aq)。向此种悬浊液中加入少量的氧化钙粉末,充分反应后恢复到原温度。下列叙述正确的是
Ca2+(aq)+2OHˉ(aq)。向此种悬浊液中加入少量的氧化钙粉末,充分反应后恢复到原温度。下列叙述正确的是
| A.溶液中钙离子数目减小 | B.溶液中钙离子浓度减少 |
| C.溶液中氢氧根离子浓度增大 | D.pH减小 |
A
解析试题分析:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,由于原溶液已经得到饱和,则反应后仍为饱和溶液,溶液各离子浓度不变,则B、C、D错误;由于反应消耗水,则溶剂质量减少,由于浓度不变,则溶液中Ca2+数减小,故A正确.
考点:难溶电解质的溶解平衡

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
下列溶液一定显酸性的是
| A.含H+的溶液 |
| B.c(OH-)<c(H+)的溶液 |
| C.pH<7的溶液 |
| D.能与金属Al反应放出H2的溶液 |
下列说法不正确的是
| A.加热或稀释NH4Cl溶液,NH4Cl水解程度均增大 |
| B.滴有酚酞试液的氨水中加入NH4Cl固体,溶液颜色变浅 |
| C.含有NH4Cl的氨水中,[NH4+]可能大于[Cl-] |
| D.纯水中加入少量NH4Cl固体,恢复到原温度,水的电离平衡右移且电离常数变大 |
下列有关电解质溶液的说法正确的是 ( )。
| A.在蒸馏水中滴加浓H2SO4,KW不变 |
| B.CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
某同学取等体积的稀盐酸与稀醋酸各一份进行稀释,下面是稀释前后的有关数据及结论,其中肯定错误的是 ( )
| | A | B | C | D |
| 稀释前 | 酸浓度相同 | 酸浓度相同 | pH均为3 | pH均为3 |
| 稀释量 | 均为10倍 | 稀释至两酸pH相同 | 稀释至pH均为5 | 均为100倍 |
| 结论 | pH:盐酸的小 | 稀释倍数:盐酸的大 | 稀释倍数:盐酸的大 | pH:盐酸的大 |
下列关于各溶液的描述中正确的是 ( )。
| A.pH相等的①NH4Cl,②(NH4)2SO4,③NH4HSO4的溶液中,c(NH4+)大小:①=②=③ |
| B.常温下,在10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20 mL |
| C.向1.00 L 0.3 mol·L-1的NaOH溶液中缓慢通入CO2气体至溶液增重8.8 g,所得溶液中:3c(Na+)=2[c(HCO3—)+c(CO32—)+c(H2CO3)] |
| D.浓度均为0.1 mol·L-1的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-) |
下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A.0.2 mol/L CH3COONa溶液和0.1 mol/L HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) |
| B.pH=3的盐酸和NaNO3的混合溶液中:c(Na+)=c(Cl-) |
| C.0.1 mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| D.物质的量浓度相等的HCN(弱酸)和NaCN溶液等体积混合后有:c(HCN)+2c(H+)=2c(OH-)+c(CN-) |
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
| 实验编号 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.2 | 0.2 | pH=9 |
| 丙 | c1 | 0.2 | pH=7 |
| 丁 | 0.2 | 0.1 | pH<7 |
下列判断正确的是( )
A.a>9
B.在乙组混合液中由水电离出的c(OH-)=10-5mol·L-1
C.c1<0.2
D.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-)