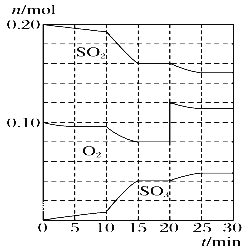
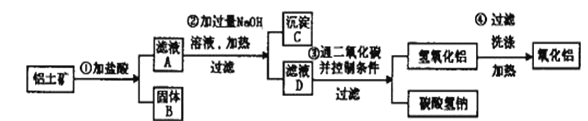
题目内容
【题目】已知: (1)Zn(s)+1/2O2(g)=ZnO(s) ΔH=-348.3 kJ/mol
(2)2Ag(s)+1/2O2(g)=Ag2O(s) ΔH=-31.0 kJ/mol
则Zn O(s)+2Ag(s)=Zn(s)+Ag2 O(s)的△H 等于()
A. -317.3kJ/mol B. -379.3kJ/mol C. +317.3kJ/mol D. -332.8kJ/mol
【答案】C
【解析】应用盖斯定律消去O2(g),将(2)式-(1)式得,ZnO(s)+2Ag(s)=Zn(s)+Ag2O(s)ΔH=(-31.0kJ/mol)-(-348.3kJ/mol)=+317.3kJ/mol,答案选C。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目