题目内容
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(Lmin).求:
(1)此时A的浓度c(A)=mol/L,反应开始前容器中的A,B的物质的量:n(A)=n(B)=mol;
(2)B的平均反应速率v(B)=mol/(Lmin);
(3)x的值为 .
【答案】
(1)0.75;3
(2)0.05
(3)2
【解析】解:(1)5min后,n(D)=0.5mol/L×2L═1mol,
根据3A(g)+B(g) ![]() xC(g)+2D(g),生成1molD要消耗1.5molA和0.5molB,
xC(g)+2D(g),生成1molD要消耗1.5molA和0.5molB,
设初始时A、B的物质的量均为n,则(n﹣1.5):(n﹣0.5)═3:5,即n=3.
c(A)═ ![]() ═0.75mol/L.故答案为:0.75;3; (2)v(B)═
═0.75mol/L.故答案为:0.75;3; (2)v(B)═ ![]() ═0.05mol/(Lmin),故答案为:0.05;(3)n(C)═0.1mol/(Lmin)×5min×2L═1mol,
═0.05mol/(Lmin),故答案为:0.05;(3)n(C)═0.1mol/(Lmin)×5min×2L═1mol,
n(D)=0.5mol/L×2L═1mol,
根据3A(g)+B(g) ![]() xC(g)+2D(g),n(C):n(D)═1:1,
xC(g)+2D(g),n(C):n(D)═1:1,
因为生成C和D的物质的量之比等化学计量数之比,所以n═2,故答案为:2.
(1)根据化学方程和物质的量浓度的计算式思考;(2)根据评价反应速率公式计算;(3)根据化学方程式计算.

【题目】减少二氧化碳的排放,氮氧化物、二氧化硫的处理与利用是一项重要的热点课题.
(1)Ⅰ.CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)C2H4(g)+4H2O(g)△H 在0.1MPa时,按n(CO2):n(H2)=1:3投料,图1所示不同温度(T)下,平衡时的四种气态物质的物质的量(n)的关系. 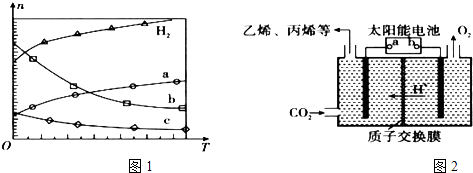
①该反应的△H0(填“>”、“=”或“<”).
②曲线b表示的物质为 .
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是 .
(2)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图2所示. b为电源的极,电解时,生成乙烯的电极反应式是 .
(3)Ⅱ.用活性炭还原法可以处理氮氧化物.如反应:C(s)+2NO(g)N2(g)+CO2(g)△H=Q kJmol﹣1 . 在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃时,该反应的平衡常数K= .
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(答一种即可).
(4)Ⅲ.工业上可以用NaOH溶液或氨水吸收过量的SO2 , 分别生成NaHSO3、NH4HSO3 , 其水溶液均呈酸性.相同条件下,同浓度的两种酸式盐的水溶液中c(SO32﹣)较小的是 , 用文字和化学用语解释原因 .


