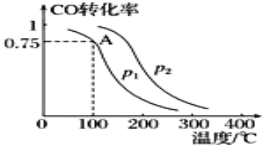
��Ŀ����
����Ŀ���������д����ĵ⣬ÿ1000g�����к���5g���ҡ�ʵ�����У��Ӻ�������ȡ��IJ�����������ͼ��

(1)�۵IJ���������________________���ݵIJ���������__________________��
(2)�Լ�b���������Ȼ�̼����������_________________________(������)��
(3)���ڢݵIJ������裬����˵����ȷ����_____________________(����ĸ)��
A. ��Һ��ʱ����Ҫ��ת��Һ©��
B. �����Һ�����Һ©������������̨�ϣ�������Һ
C. ��Һʱ�����²�Һ�嶼Ҫ�ӷ�Һ©���¿������ձ��ڱ����벻ͬ���ձ�
D. ��Һʱ����Ҫ������Һ©���Ϸ��IJ�������ʹ��Һ©���ܷ�
(4)�Լ�a��ѡ��ϡ�����ữ�Ĺ���������Һ����ȫ����ܷ�Ӧ�����ӷ���ʽ��___I�D +____H2O2+______==____I2+______��(ϵ��Ϊ��1��ʱ��Ҫд��1��)
(5)ij��ȤС�����ʵ�鷽�����Ӻ�I2��CCl4��Һ�з���I2��CCl4����֪��
�۵� | �е� | |
I2 | 114�� | 184�� |
CCl4 | -23�� | 77�� |
��С��ͬѧ�������ϣ�����������ķ�������װ������ͼװ�ã�����B��������_____��ͼ����һ�����Դ���Ӧ����Ϊ_______________________________________��
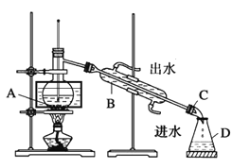
�ڸ�С��ͬѧ����װ�ô������ʵ�顣��80��ˮԡ����Ƭ�̣��۲쵽��ƿ�г�����ɫ��������ƿ��Ҳ��ʼ�ռ���dz�Ϻ�ɫ��Һ��������ƿ�в���������I2��ͨ��ʵ��ó����ۣ���ѹ�µ�����__________________________(�����ʺ����������ʺ���)����I2��CCl4��
���𰸡����� ��ȡ��Һ �������� A 2 1 2H+ 1 2H2O ������ �¶ȼƵ�ˮ������������ƿ��֧�ܿڴ� ���ʺ�
��������
������Ҫ���麣ˮ����ȡ�ⵥ�ʵ�ʵ����������ز�����
��1��������Ϊ��Һ���������������ΪҺҺ�����ܷ��������
��2�����ݳ�����ȡʵ������ȡ����ѡ��ԭ�������
��3�����ݷ�Һ�ľ��������ɣ�
��4������������ԭ��Ӧ���ϼ���������Լ�ԭ���غ㡢����غ���ƽ��
��5���ٸ���ʵ���ҳ�������������д����������ʵ�����¶ȼƵ�ˮ����λ����д��
�ڵⵥ��������������80��ʱ������CCl4һ�������ƿ�У��ɴ������жϡ�
��1��������Ϊ��Һ�����ܷ���������ʲ�������Ϊ���ˣ�������ΪҺҺ�����ܷ���������ʲ�������Ϊ��Һ��
��2���Լ�bΪ��ȡ������ʵ���л���ѡ�ñ������ͣ�
��3��������Ϊ��Һ��A.��Һ��ʱ����Ҫ��ת��Һ©�����Ա�֤��ȡ����������ȫ�Ӵ��������ȡ�ʣ���ȷ��B.�����Һ�����Һ©������������̨�ϣ�����������Һ��ȫ�ֲ�ʱ���ٽ��з�Һ������C.��Һʱ���ϲ�Һ����Ͽڵ������²�Һ��ӷ�Һ©���¿������������Լ�����Ⱦ������D.��Һʱ�����²�Һ������У��轫©���ϿڵIJ�������ʹ���ϵİ��ۻ�С��©�����ϵ�С�ף�ʹ©�����������ͨ���Ա�֤�²�Һ����˳��������������
��4���÷�Ӧ��H2O2��������������Oȫ����-1�۽���Ϊ-2�ۣ�I-��-1������Ϊ0�ۣ��÷�Ӧ�������Ի����½��У�����������ԭ��Ӧ���ϼ�������ȿ�֪���÷�Ӧ�����ӷ���ʽΪ��2I- + H2O2 + 2H+ ===I2 + 2H2O��
��5��������BΪ�����ܣ�����ʵ���У���ԭ���Ǹ���Һ��ķе������з��룬����ͨ���¶ȼƲ������Һ�������¶ȣ����¶ȼƵ�ˮ����Ӧ��֧�ܿ���ƽ�У�
���������Ϣ��֪��CCl4��80��ʱΪ��̬����I2��������������CCl4����һ�������ƿ�����ܴﵽ����I2��CCl4��ʵ��Ŀ�ġ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��ijС���о�NaClO��Һ��KI��Һ�ķ�Ӧ��ʵ���¼���£�
ʵ���� | ʵ����� | ʵ������ |
�� |
| ������Һ��Ϊdz��ɫ ������Һ���� |
�� |
| ������Һ������ɫ ������Һ����������Һ��pH=10 |
������������Ļ�������Ҫ��I��IO3����ʽ����������������IO3��������Cl����������I��ClO��pH<4�����ȵ������¼����ȶ���
��1��0.5 mol��L1 NaClO��Һ��pH��11�������ӷ���ʽ��ʾ��ԭ����______��
��2��ʵ��������Һ��Ϊdz��ɫ�����ӷ���ʽ��______��
��3���Ա�ʵ�����͢��о�ʵ������Ӧ������Һ����������ԭ��
�� �������a��I2�ڼ�����Һ�в��ܴ��ڡ����ʵ����֤ʵ�˼���a������ʵ���IJ�����������______��
�� ��һ���������b��NaClO�ɽ�I2����ΪIO3������ʵ��֤ʵ�˼���b������װ������ͼ�����м���Һ��______��ʵ��������______��

��4������ʵ���������Һ�е�IO3��
ȡʵ����������Һ���μ�ϡ�������������������̾�δ������ɫ��һ��ʱ����л���ɫ�̼�����ζ����������������Һ��pH��2���ټ���KI��Һ����Һ������˵��ʵ����������Һ�д���IO3��
�� �����Ļ���ɫ������______��
�� ��ͬѧ��Ϊ��ʵ�鲻��˵��ʵ���������Һ�д���IO3��������______����֤��ʵ����������Һ�д���IO3���Ľ���ʵ�鷽����______��
�� ʵ�����з�Ӧ�����ӷ���ʽ��______��