题目内容
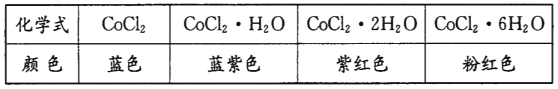
【题目】25℃时,四种均为0.1molL﹣1的溶液,其pH如下表所示:
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaHCO3 |
|
pH | 7.0 | 7.0 | 8.4 | 9.9 |
下列关系不正确的是
A. 酸性:H2CO3 > ![]()
B. 水电离产生的c(H+):① = ②
C. 溶液③中:c(HCO3﹣)+ c(CO32﹣)+ c(H2CO3)= 0.1molL﹣1
D. 溶液④中:c(Na+)> c(![]() )> c(OH-)> c(H+)
)> c(OH-)> c(H+)
【答案】B
【解析】A.碳酸氢钠溶液的pH小于苯酚钠,说明碳酸氢根的水解程度小于苯酚钠,则酸性:H2CO3> ![]() >NaHCO3,A正确;B.氯化钠不水解,不影响水的电离,醋酸铵水解促进水的电离,则水电离产生的c(H+):①<②,B错误;C.溶液③中根据物料守恒可知c(HCO3﹣)+ c(CO32﹣)+ c(H2CO3)=0.1molL﹣1,C正确;D.苯酚钠水解溶液显碱性,则溶液④中:c(Na+)>c(
>NaHCO3,A正确;B.氯化钠不水解,不影响水的电离,醋酸铵水解促进水的电离,则水电离产生的c(H+):①<②,B错误;C.溶液③中根据物料守恒可知c(HCO3﹣)+ c(CO32﹣)+ c(H2CO3)=0.1molL﹣1,C正确;D.苯酚钠水解溶液显碱性,则溶液④中:c(Na+)>c(![]() )>c(OH-)>c(H+),D正确,答案选B。
)>c(OH-)>c(H+),D正确,答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目