题目内容
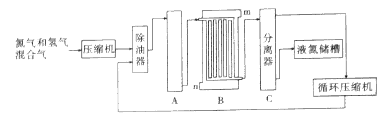
【题目】合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.利用N2和H2合成氨,目前工业的生产条件为:催化剂(铁触媒),温度(400~500℃),压强(30~50MPa),如图为流程示意图:
请回答下列问题:
(1)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是__________,__________;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式__________,__________;
(2)设备A中含有电加热器、铁触煤和热交换器,设备A的名称__________,其中发生的化学反应方程式为__________;实际生产中采用400~500℃的高温,原因之一是__________,原因之二是__________。
(3)设备B的名称__________,其中m和n是两个通水口,入水口是__________(填“m”或“n”).不宜从相反方向通水的原因是__________;
(4)设备C的作用__________;
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g)![]() CO2(g)+H2(g),已知1000K时该反应的平衡常数K=1,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于__________。
CO2(g)+H2(g),已知1000K时该反应的平衡常数K=1,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于__________。
【答案】
(1)液化、分馏 与碳反应后除去CO2
C+H2O![]() CO+H2 CH4+H2O
CO+H2 CH4+H2O![]() CO+3H2
CO+3H2
(2)合成(氨)塔 N2+3H2![]() 2NH3(必须注明反应条件)
2NH3(必须注明反应条件)
温度太低,反应速率慢,温度太高,平衡逆向移动;在400~500℃时催化剂的活性最高
(3)冷却塔(或冷凝器) n 高温气体由冷却塔的上端进入,冷却水从下端进入,逆向冷却效果好
(4)将液氨与未反应的原料气分离
(5)9
【解析】
试题分析:(1)分离空气提取氮气的方法有两种,以上液化、分馏空气,另一种为空气与碳反应生成二氧化碳,反应后除去二氧化碳气体;C和水反应的方程式为C+H2O![]() CO+H2,甲烷与水反应的方程式为CH4+H2O
CO+H2,甲烷与水反应的方程式为CH4+H2O![]() CO+3H2,故答案为:液化、分馏;与碳反应后除去CO2;C+H2O
CO+3H2,故答案为:液化、分馏;与碳反应后除去CO2;C+H2O![]() CO+H2;CH4+H2O
CO+H2;CH4+H2O![]() CO+3H2;
CO+3H2;
(2)合成氨的设备为合成塔,发生N2(g)+3H2(g)![]() 2NH3(g),实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,升高温度虽然不利于平衡向正反应方向移动,但能增大反应速率,缩短达到平衡的时间,这是原因之二,故答案为:合成(氨)塔;N2(g)+3H2(g)
2NH3(g),实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,升高温度虽然不利于平衡向正反应方向移动,但能增大反应速率,缩短达到平衡的时间,这是原因之二,故答案为:合成(氨)塔;N2(g)+3H2(g)![]() 2NH3(g);催化剂的催化活性;增加反应速率,缩短达到平衡的时间;
2NH3(g);催化剂的催化活性;增加反应速率,缩短达到平衡的时间;
(3)冷凝分离设备为冷凝塔或冷凝器,水流和气流方向应逆向,则入水口是n,高温气体由冷凝塔上端进入,冷凝水从下端进入,可使冷水充满冷凝器,逆向冷凝效果好,故答案为:冷凝塔或冷凝器;n;高温气体由冷凝塔上端进入,冷凝水从下端进入,逆向冷凝效果好;
(4)分离器用来分离液氨和原料气,故答案为:将液氨与未反应的原料气分离;
(5)设CO、H2O起始物质的量浓度分别为x和y,按CO的转化率为90%计算,则
CO(g) + H2O(g)![]() CO2(g) + H2(g)
CO2(g) + H2(g)
起始浓度: x y 0 0
转化浓度: 0.9x 0.9x 0.9x 0.9x
平衡浓度: 0.1x ![]() 0.9x 0.9x
0.9x 0.9x
根据![]() ,求得
,求得![]() 。只要y∶x不低于9,CO的转化率便会超过90%。故答案为:9。
。只要y∶x不低于9,CO的转化率便会超过90%。故答案为:9。