题目内容
10.已知25℃时,下列酸的电离常数:醋酸(CH3COOH):1.75×10-5,氢氰酸(HCN):4.93×10-10,氢氟酸(HF)7.2×10-4,甲酸(HCOOH):1.77×10-4.物质的量浓度均为0.1mol•L-1的上述溶液,酸性最强的是( )| A. | 醋酸 | B. | 氢氰酸 | C. | 氢氟酸 | D. | 甲酸 |
分析 相同浓度的酸,酸的电离常数越大,酸性越强,据此分析解答.
解答 解:相同浓度的酸,酸的电离常数越大,说明酸的电离程度越大,则酸的酸性越强,根据题意知,氢氟酸的电离平衡常数最大,所以氢氟酸的酸性最强,故选C.
点评 本题考查弱电解质的电离,题目难度不大,本题注意电离平衡常数与酸性的强弱判断.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
11.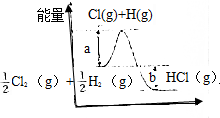 氢气在氯气中燃烧的化学方程式为$\frac{1}{2}$Cl2 (g)+$\frac{1}{2}$H2 (g)═HCl(g),该反应过程中的能量变化如图所示,下列有关叙述正确的是( )
氢气在氯气中燃烧的化学方程式为$\frac{1}{2}$Cl2 (g)+$\frac{1}{2}$H2 (g)═HCl(g),该反应过程中的能量变化如图所示,下列有关叙述正确的是( )
 氢气在氯气中燃烧的化学方程式为$\frac{1}{2}$Cl2 (g)+$\frac{1}{2}$H2 (g)═HCl(g),该反应过程中的能量变化如图所示,下列有关叙述正确的是( )
氢气在氯气中燃烧的化学方程式为$\frac{1}{2}$Cl2 (g)+$\frac{1}{2}$H2 (g)═HCl(g),该反应过程中的能量变化如图所示,下列有关叙述正确的是( )| A. | a代表反应物的总能量 | B. | a+b代表生成物的总能量 | ||
| C. | 该反应为放热反应 | D. | 反应焓变△H=bkJ•mol-1 (b>0) |
1.下列化学用语表达方式正确的是( )
| A. | 碳-12符号:612C | B. | 氯化氢电子式: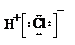 | ||
| C. | 次氯酸结构式:H-Cl-O | D. | 氯化镁电子式: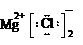 |
18.“可燃冰”它的主要成分是甲烷与水分子的结晶水合物(CH4•nH20).其形成:埋于海底地层深处的大量有机质在缺氧环境中,厌氧性细菌把有机质分解,最后形成石油和天然气(石油气),其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”.又知甲烷同C02一样也是温室气体.这种可燃冰的晶体类型是( )
| A. | 离子晶体 | B. | 分子晶体 | C. | 原子晶体 | D. | 金属晶体 |
5.某种烃与H21:1加成后的产物是(CH3)2CHCH(CH3)C(CH3)3则该烃的结构式可能有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
15.对于反应2NO2(g)?N2O4(g),在一定条件下达到平衡,在温度不变时,欲使n(NO2)与n(N2O4)的比值增大,应采取的措施是:①体积不变,增加NO2质的量;②体积不变,增加N2O4质的量;③使体积增大到原来的2倍;④充入N2保持压强不变( )
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
2.将等物质的量的SO2、Cl2通入水中,所得溶液( )
| A. | 呈中性,有漂白性 | B. | 呈酸性,有漂白性 | C. | 只有漂白性 | D. | 呈酸性,无漂白性 |
20.现要制备无水FeCl3,并将其保存下来,能选用的仪器或装置如图所示:
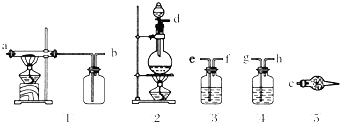
供选用的试剂如下:
A.食盐晶体 B水 C.饱和食盐水 D.烧碱溶液 E.铁粉
F.二氧化锰 G.浓硫酸 H.无水CaCl2 I.碱石灰
(1)从上述仪器中选取若干连成一个制备并保存无水FeCl3的装置,用图中各管口标号按先后可连接为d接e,f接g,h接a,b接c;
(2)填写连接装置中各选用仪器里应盛放的物质:
(3)是否需要选择装置⑤要,其原因是FeCl3易吸收空气中的水而水解,多余的Cl2可污染空气.

供选用的试剂如下:
A.食盐晶体 B水 C.饱和食盐水 D.烧碱溶液 E.铁粉
F.二氧化锰 G.浓硫酸 H.无水CaCl2 I.碱石灰
(1)从上述仪器中选取若干连成一个制备并保存无水FeCl3的装置,用图中各管口标号按先后可连接为d接e,f接g,h接a,b接c;
(2)填写连接装置中各选用仪器里应盛放的物质:
| 仪器标号 | |||||
| 试剂标号 |
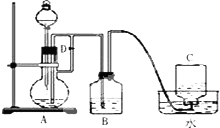 由于Fe(OH)2在空气中易被氧化,为了观察到白色的Fe (OH)2想了很多方法.
由于Fe(OH)2在空气中易被氧化,为了观察到白色的Fe (OH)2想了很多方法.