题目内容
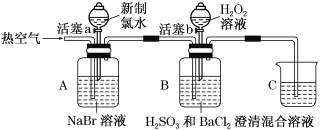
【题目】某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加少量新制氯水,关闭活塞a | A中溶液变为浅红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | B中开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)实验操作Ⅰ时,A中反应的离子方程式为__________________________。
(2)实验操作Ⅱ吹入热空气的目的是________________________________。
(3)装置C的作用是______________________;C中盛放的药品是________。
(4)实验操作Ⅲ中混合液逐渐变成红棕色,其对应的离子方程式为_____________。
(5)由上述实验得出的结论是______________________________________。
(6)①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否有干扰,理由是_______________________________________________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是________________(写出一条即可)。
【答案】2Br-+Cl2===Br2+2Cl-吹出单质Br2吸收多余的Br2,以免污染环境NaOH溶液H2O2+2Br-+2H+===Br2+2H2O氧化性:H2O2>Br2>H2SO3不干扰,无论热空气是否参加氧化H2SO3,只要观察到B中产生白色沉淀的同时颜色无明显变化,即能证明Br2氧化了H2SO3H2SO3有剩余(或H2O2浓度小或Br-与H2O2反应慢等合理答案均可)
【解析】
(1)A中是氯水滴入溴化钠溶液中发生 的氧化还原反应,氯气氧化溴离子为溴单质,A中溶液变为红棕色.反应的离子方程式为:2Br-+Cl2=Br2+2Cl-,故答案为:2Br-+Cl2=Br2+2Cl-;
(2)吹入热空气,A中红棕色明显变浅,说明溴单质被赶入B在;B中有气泡,产生大量白色沉淀,说明溴单质氧化亚硫酸生成硫酸和氯化钡生成白色沉淀,混合液颜色无明显变化,进一步证明了溴单质被还原为溴离子,故答案为:吹出单质Br2;
(3)装置C是尾气吸收装置,反应过程中有氯气、溴蒸气等污染性气体不能排放到空气中需要用氢氧化钠溶液吸收,故答案为:吸收尾气;NaOH溶液;
(4)滴入过氧化氢在酸溶液中会氧化溴离子为溴单质,反应的两种方程式根据电子守恒、原子守恒配平书写为:H2O2+2Br-+2H+=Br2+2H2O,故答案为:H2O2+2Br-+2H+=Br2+2H2O;
(5)依据反应H2SO3+Br2+H2O=H2SO4+2HBr;H2O2+2Br-+2H+=Br2+2H2O;氧化还原反应中 氧化剂的氧化性大于氧化产物,氧化性为:H2O2>Br2>H2SO3,故答案为:氧化性为H2O2>Br2>H2SO3;
(6)①欲证明是H2SO3与Br2发生了反应,有两个角度:H2SO3被氧化→有SO42-,即沉淀 Br2被还原→有Br-且颜色不变化,其中第一条有氧气的干扰,但第二条完全符合实验现象,故已经可以说明是H2SO3而非氧气与Br2发生了反应,故答案为:不干扰,无论热空气是否参加氧化H2SO3,只要观察到产生白色沉淀的同时无明显颜色变化,即能证明Br2氧化了H2SO3;
②实验操作III,开始时颜色无明显变化的原因是,氯化铁浓度小、过氧化氢与溴离子反应慢,亚硫酸有剩余等,故答案为:H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可)。