题目内容
(12分)
(1)现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
① 酸式滴定管用蒸馏水洗净后,还应该进行的操作是_______________________。
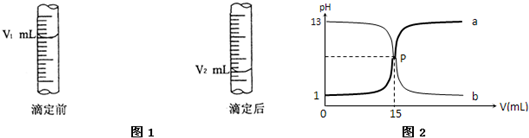
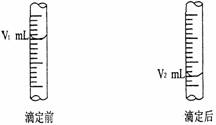 ② 右图是酸式滴定管中液面在滴定前后的读数:
② 右图是酸式滴定管中液面在滴定前后的读数:
试用有关符号表示该待测NaOH溶液的物质的量
浓度:c (NaOH) = _________________ mol/L。
③ 若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会偏_________________。
(2) 已知空气中含有N2、O2、CO2、H2S等气体。试判断下列滴定操作的终点、分析出现下列现象的原因。(或用有关离子方程式表示)
① 以酚酞为指示剂,用碱液滴定酸液到 为终点。约半分钟后导致褪色的原因: 。
② 以淀粉为指示剂,用Na2S2O3滴定I2(2S2O32—+I2 = S4O62—+2I—)到 为终点,约5min后溶液又显色的原因: 。
(1)(6分)①用已知物质的量浓度的标准盐酸润洗2到3次
②c (NaOH) = (V2-V1)a/V ③高 (各2分)
(2)(6分) ①显现浅红色且在半分钟内不褪色;(1分) 空气中存在CO2 、H2S , CO2+OH—==HCO3—, H2S+OH—==HS—+H2O(2分,叙述合理即可,下同)
② 蓝色恰好褪去;(1分) 空气中存在O2; O2+4I—+4H+===2H2O+I2(2分)