题目内容
【题目】海洋中有丰富的食品、矿产、能源、药物和水产等资源,如图表示海水综合利用的部分过程.下列说法不正确的是( ) 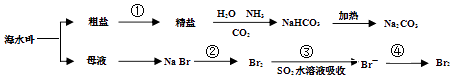
A.工业上通过电解熔融状态MgCl2制取金属镁
B.用澄清石灰水可鉴别NaHCO3和Na2CO3
C.在第②、④步骤中,溴元素均被氧化
D.制取NaHCO3的反应中,利用了其溶解度在相同条件下小于NaCl的性质
【答案】B
【解析】解:A、工业上是电解熔融的氯化镁来制取金属镁,故A正确; B、碳酸钠、碳酸氢钠和氢氧化钙之间均能反应,且都会出现白色沉淀,所以用澄清的石灰水不可鉴别NaHCO3和Na2CO3 , 故B错误;
C、第②步中,溴元素化合价从﹣1升高到0价,被氧化,第④步中,溴元素化合价从﹣1升高到0价,被氧化,故C正确;
D、向饱和食盐水中通入氨气以及二氧化碳,溶解度较小的碳酸氢钠会先析出,制取NaHCO3的反应是利用其溶解度小于NaCl,故D正确;
故选B.

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案【题目】碳酸锂(相对分子质量74)广泛应用于化工、冶金等行业.工业上利用锂辉石(Li2Al2Si4Ox)制备碳酸锂的流程如图: 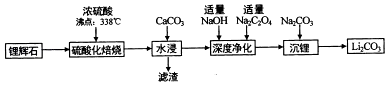
已知:碳酸锂的溶解度为((g/L)
温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
请回答下列问题:
(1)锂辉(Li2Al2Si4Ox)可以用氧化物的形式表示其组成,形式为
(2)硫酸化焙烧温度控制在250℃﹣300℃之间,主要原因是 . 焙烧中硫酸用量控制在理论用最的l15%左右,硫酸加入过多的副作用是 .
(3)水浸时,加入CaCO3粉末充分反应后过滤,滤渣的主要成分除CaCO3外还有 .
(4)“沉锂”的化学反应方程式为 .
(5)“沉锂”需要在95℃以上进行,主耍原因是 . 过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有和 .