题目内容
4.一个原电池反应为:Zn+Cu2+═Zn2++Cu,该原电池的电极及电解质溶液可能是( )| 正极 | 负极 | 电解质溶液 | |
| A | Cu | Zn | CuSO4溶液 |
| B | Cu | Zn | 稀H2SO4 |
| C | Cu | Zn | ZnCl2溶液 |
| D | 石墨 | Zn | CuCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据电池反应式知,失电子的金属作负极,则锌作负极,不如负极活泼的金属或导电的非金属作正极,铜离子得电子发生还原反应,所以电解质溶液中含有铜离子,则电解质溶液为可溶性的铜盐.
解答 解:锌失电子发生氧化反应而作负极,不如锌活泼的金属或导电的非金属作正极(石墨),铜离子在正极上得电子发生还原反应,则电解质为可溶性的铜盐,符合条件的是AD,故选AD.
点评 本题考查了原电池工作原理,判断正负极、电解质溶液时,要根据电池反应式判断:发生氧化反应的电极为负极,发生还原反应的电极为正极,含有发生还原反应的离子溶液为电解质溶液.

练习册系列答案
相关题目
15.下列有关化学实验安全问题的叙述中,不正确的是( )
| A. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 取用化学药品时,应特别注意观察药品包装容器上的安全警示标志 | |
| C. | 凡是给玻璃仪器加热,都要加垫石棉网,以防止仪器炸裂 | |
| D. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
12.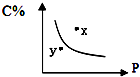 对于mA(s)+nB(g)?pC(g)的可逆反应,在一定温度下C的百分含量与压强的关系如图所示,则下列判断正确的是( )
对于mA(s)+nB(g)?pC(g)的可逆反应,在一定温度下C的百分含量与压强的关系如图所示,则下列判断正确的是( )
 对于mA(s)+nB(g)?pC(g)的可逆反应,在一定温度下C的百分含量与压强的关系如图所示,则下列判断正确的是( )
对于mA(s)+nB(g)?pC(g)的可逆反应,在一定温度下C的百分含量与压强的关系如图所示,则下列判断正确的是( )| A. | m+n<p | B. | n>p | ||
| C. | x点的状态是v正>v逆 | D. | y点的状态是v正>v逆 |
19.用导线将铜片和锌片连接后插入稀硫酸中组成原电池,其中铜片作( )
| A. | 阳极 | B. | 阴极 | C. | 正极 | D. | 负极 |
16.下列反应的离子方程式不正确的是( )
| A. | 碳酸氢钠溶于盐酸:HCO3-+H+═H2O+CO2↑ | |
| B. | 硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ | |
| C. | 氢氧化铝中和胃酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | 硝酸银溶液中加入铜粉:Ag++Cu═Cu2++Ag |
13.在373K时,密闭容器中充入一定量的NO2和SO2,发生如下反应:NO2+SO2?NO+SO3,下列叙述正确的是( )
| A. | 在任何时刻NO2和SO3的物质的量一定相等 | |
| B. | 在平衡状态时NO2和SO2的物质的量一定相等 | |
| C. | 在任何时刻体系中的总物质的量一定等于反应开始时总物质的量 | |
| D. | 在平衡状态时SO2、NO2、NO、SO3的物质的量一定相等 |
14.下列说法不正确的是( )
| A. | 天然蛋白质水解的最终产物是a-氨基酸 | |
| B. | CuSO4溶液会使蛋白质发生变性 | |
| C. | 凡含有“-CONH-”的化合物均为蛋白质 | |
| D. | 浓HNO3会使某些蛋白质变黄 |