题目内容
将一小块固体钠在空气中加热片刻,然后将固体投入足量的水中,产生V mL(标准状况下)气体,向余下的溶液中加入10 mL 6 mol·L-1的盐酸恰好中和。
(1)求原固体钠的质量。
(2)若V="336" mL,且反应产生的气体经点燃恰好完全反应,那么在空气中加热后所得到的固体其所含成分的质量分别为多少?
(1)求原固体钠的质量。
(2)若V="336" mL,且反应产生的气体经点燃恰好完全反应,那么在空气中加热后所得到的固体其所含成分的质量分别为多少?
(1)1.38 g
(2)m(Na)=" 0.46" g
m(Na2O2) ="0.78" gm(Na2O)="0.62" g
(2)m(Na)=" 0.46" g
m(Na2O2) ="0.78" gm(Na2O)="0.62" g
(1)固体与水反应后所得的溶液为NaOH溶液,2Na+2H2O====2NaOH+H2↑,2Na2O2+2H2O====4NaOH+O2↑,Na2O+H2O====2NaOH。再由NaOH+HCl====NaCl+H2O,可知盐酸的物质的量与一开始钠的物质的量是相同的,即n(Na)="n(HCl)=0.01" L×6 mol·L-1="0.06" mol,m(Na)="0.06" mol×23 g·mol-1="1.38" g。
(2)336 mL的气体应为H2和O2的混合物,由?2H2+O2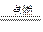 2H2O可知?V(H2)="224" mL,V(O2)=?112 mL,即n(H2)="0.01" mol,n(O2)="0.005" mol。
2H2O可知?V(H2)="224" mL,V(O2)=?112 mL,即n(H2)="0.01" mol,n(O2)="0.005" mol。
2Na+2H2O====2NaOH+H2↑
2 mol 1 mol
0.02 mol 0.01 mol
2Na2O2+2H2O====4NaOH+O2↑
2 mol 1 mol
0.01 mol 0.005 mol
则加热后的固体中
n(Na2O)=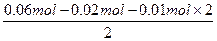 ="0.01" mol
="0.01" mol
m(Na)="0.02" mol×23 g·mol-1="0.46" g
m(Na2O2)="0.01" mol×78 g·mol-1="0.78" g
m(Na2O)="0.01" mol×62 g·mol-1="0.62" g
(2)336 mL的气体应为H2和O2的混合物,由?2H2+O2
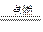 2H2O可知?V(H2)="224" mL,V(O2)=?112 mL,即n(H2)="0.01" mol,n(O2)="0.005" mol。
2H2O可知?V(H2)="224" mL,V(O2)=?112 mL,即n(H2)="0.01" mol,n(O2)="0.005" mol。2Na+2H2O====2NaOH+H2↑
2 mol 1 mol
0.02 mol 0.01 mol
2Na2O2+2H2O====4NaOH+O2↑
2 mol 1 mol
0.01 mol 0.005 mol
则加热后的固体中
n(Na2O)=
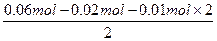 ="0.01" mol
="0.01" molm(Na)="0.02" mol×23 g·mol-1="0.46" g
m(Na2O2)="0.01" mol×78 g·mol-1="0.78" g
m(Na2O)="0.01" mol×62 g·mol-1="0.62" g

练习册系列答案
相关题目